a Никита Бучинский 1 éve
228
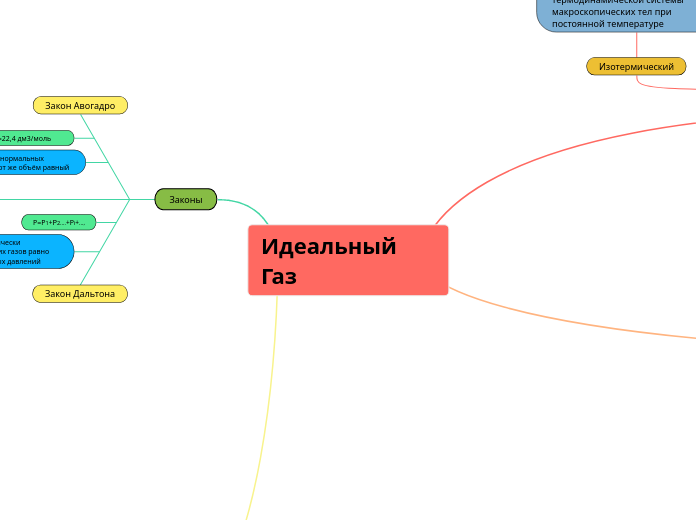
Идеальный Газ
Идеальный газ подчиняется ряду уравнений и законов, которые описывают его поведение при различных условиях. Основные уравнения состояния идеального газа включают уравнение Клапейрона и уравнение Менделеева, которые связывают давление, объем и температуру.