a lian rey 1 éve
177
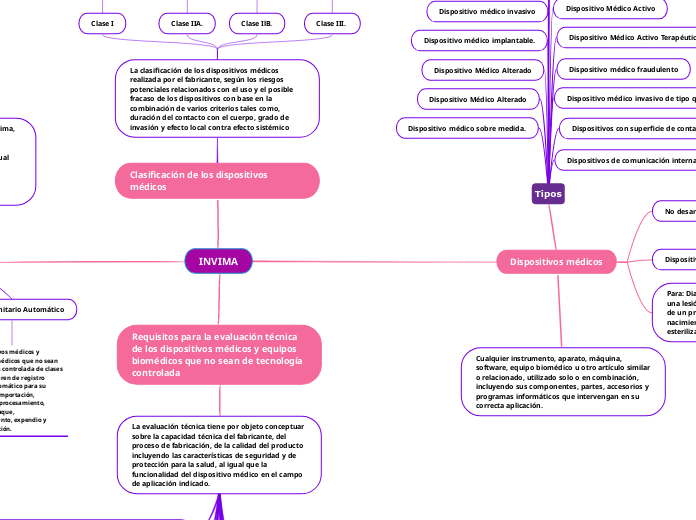
INVIMA
Los dispositivos médicos son esenciales para una variedad de funciones que no implican una acción terapéutica directa. Estos dispositivos se utilizan para el diagnóstico, prevención, supervisión o alivio de enfermedades, así como para el tratamiento y compensación de lesiones o deficiencias.