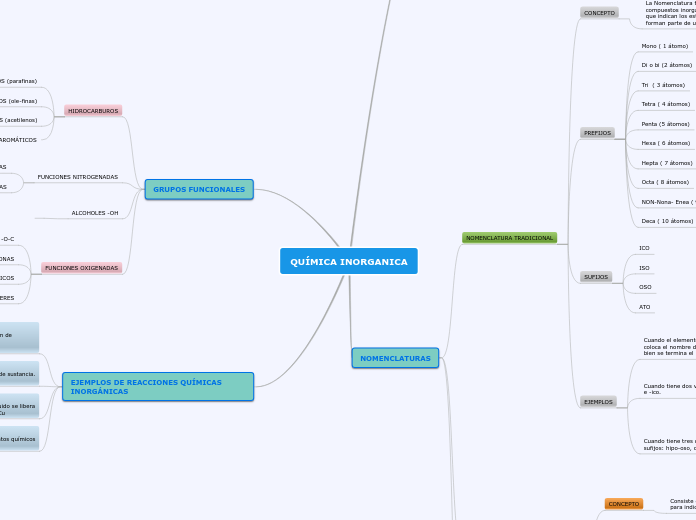
QUÍMICA INORGANICA
EJEMPLOS DE REACCIONES QUÍMICAS INORGÁNICAS
Doble sustitución.
Intercambio entre los elementos químicos
H2SO4+NaCl→HCl+Na2SO4
Sustitución.
El componente sustituido se libera
Fe+CuSO4→FeSO4+Cu
Descomposición.
Por desdoblamiento o reactivo de sustancia.
CaCo3→CaO+CO2
Síntesis.
Se obtiene un producto diferente de la combinación de reactivos.
Ca+2H2O→Ca(OH)2+H2↑
GRUPOS FUNCIONALES
FUNCIONES OXIGENADAS
ÉSTERES
ÁCIDOS CARBOXÍLICOS
CETONAS
ÉTERES -O-C
ALCOHOLES -OH
FUNCIONES NITROGENADAS
*AMIDAS
*AMINAS
HIDROCARBUROS
AROMÁTICOS
ALQUINOS (acetilenos)
-C=C-
ALQUENOS (ole-finas)
GRUPO FUNCIONAL
>C=C<
ALCANOS (parafinas)
NO TIENE GRUPO FUNCIONAL
NOMENCLATURAS
NOMENCLATURA DE STOCK
Ca0
óxido de calcio
Fe203
Óxido de hierro (III)
Se coloca el número de oxidación del elemento en números romanos entre paréntesis y después del nombre
Se indica primero la palabra óxido, seguida del nombre del otro constituyente.
NOMENCLATURA SISTEMÁTICA O IUPAC
FE2O3
Trióxido de dihierro
PREFIJOS UTILIZADOS
Momo (1)
di (2)
tri (3)
tetra (4)
penta (5)
hexa (6)
hepta (7)...
Consiste en la utilización de prefijos numerales griegos
para indicar el número de átomos de cada elemento
NOMENCLATURA TRADICIONAL
EJEMPLOS
Cuando tiene tres distintas valencias se usan los prefijos y sufijos: hipo-oso, oso, ico.
El titanio presenta tres valencias: 2,3,4. Para la valencia menor se usa hipo-oso, para la valencia intermedia se utiliza el sufijo oso y para la valencia mayor se emplea ico.
TiO óxido hipotitanioso
Ti2O3 óxido titanioso
Ti2O4 = TiO2 óxido titánico
Cuando tiene dos valencias diferentes se usan los sufijos -oso e -ico.
El hierro tiene dos valencias: 2 y 3. Para la valencia menor se coloca el sufijo oso y para la valencia mayor el sufijo ico.
FeCl2 Cloruro ferroso
Cuando el elemento solo tiene una valencia, simplemente se coloca el nombre del elemento precedido de la sílaba “de” o bien se termina el nombre del elemento con el sufijo –ico.
K2O óxido de potasio / óxido potásico
Mg(OH)2 Hidróxido de magnesio / Hidróxido magnésico
CaH2 Hidruro de calcio / Hidruro cálcico
SUFIJOS
ATO
OSO
ISO
ICO
PREFIJOS
Deca ( 10 átomos)
NON-Nona- Enea ( 9 átomos)
Octa ( 8 átomos)
Hepta ( 7 átomos)
Hexa ( 6 átomos)
Penta (5 átomos)
Tetra ( 4 átomos)
Tri ( 3 átomos)
Di o bi (2 átomos)
Mono ( 1 átomo)
CONCEPTO
La Nomenclatura tradicional se basa en nombrar a los compuestos inorgánicos, utilizando prefijos y sufijos griegos que indican los estados de oxidación de los elementos que forman parte de un compuesto.
CARACTERÍSTICAS
PESO MOLECULAR
BAJO PESO MOLECULAR
TIPOS DE ENLACE
IÓNICO
Red Iónica
Ejemplo:Cloruro de Potasio, KC1
COVALENTE
Moléculas gigantes
Ejemplo: Diamante, C
Moléculas simples
Ejemplo: Metano, CH4
ELEMENTOS
TODOS LOS ELEMENTOS DE LA TABLA PERIÓDICA
COMPUESTOS
HIDRURO
SAL
HIDRÓXIDOS
ANHÍDRIDOS
OXIDOS
SOLUBLES
RESISTENCIA AL CALOR