da CRISTIAN SANTIAGO ACOSTA LOZANO mancano 3 anni
255
Organigrama
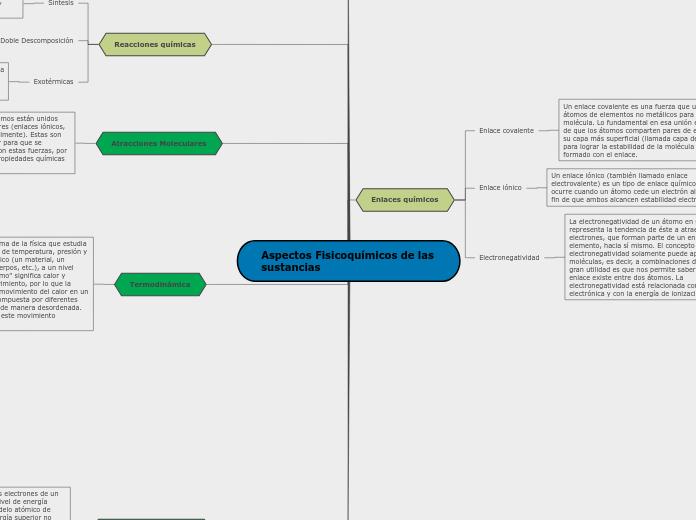
La electronegatividad es una medida clave que determina la capacidad de un átomo para atraer electrones en una molécula, influyendo así en el tipo de enlace que se forma entre átomos.
da CRISTIAN SANTIAGO ACOSTA LOZANO mancano 3 anni
255

Più simili a questo