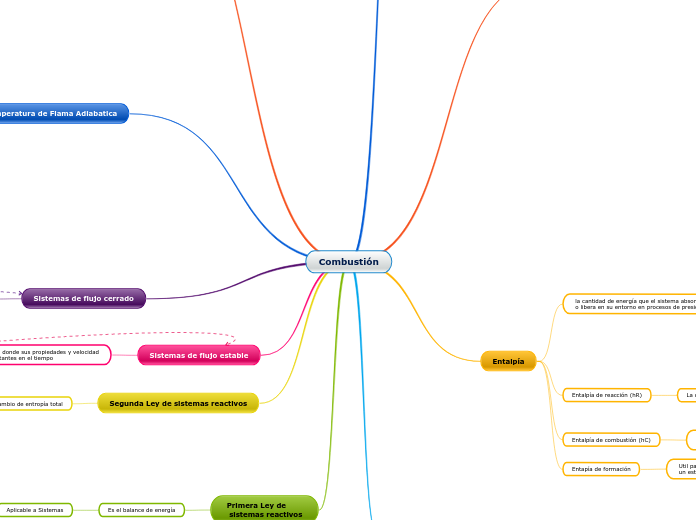
Combustión
Primera Ley de
sistemas reactivos
Es el balance de energía
Aplicable a Sistemas
No reactivos
Reactivos
Se debe tener en consideración
cosas importantes
Saber si combustible y aire ingresan
a la cámara de combustión
Premezclados o separadamente
Por ejemplo el estado del
combustible.
gas
sólido
De este estado depende la
entalpía de formación h°f
Depende de la fase de
combustible
líquido
Los que son químicamente reactivos
implican cambios de energía
Por lo que es mejor reescribir
relaciones de balance y energía
Para sistemas
Cerrados
De Flujo estable
Segunda Ley de sistemas reactivos
Ya evaluado el cambio de entropía total
La exergía destruida: X destruida asociada con
reacción química
Se determina: Xdestruida = T0 Sgen (KJ)
Donde T0 es la temperatura absoluta
de los alrededores
Sistemas de flujo estable
Flujo continuo en donde sus propiedades y velocidad
permanecen constantes en el tiempo
La ecuación de continuidad en
flujo estable esta dada por:
w= AV/v
v= vol especifico del flujo que avanza
V= Velocidad media a través del área
donde A= área de la sección
Sistemas de flujo cerrado
La relación general de balance de energía para un sistema cerrado es Eentrada - Esalida = ∆Esistema
se expresa para un sistema cerrado químicamente reactivo
estacionario
Como: (Q ent -Q sal) + (W ent - W sal) = U prod - U react (kJ / kmol combustible)
Temperatura de Flama Adiabatica
Su temperatura es más baja que el proceso a presión constante porque parte de la energía se utiliza para cambiar el volumen del sistema
es la temperatura que resulta de un proceso de combustión completa que ocurre sin cualquier trabajo, transferencia de calor o cambios en cinética o energía potencial.
determinación de la temperatura de flama adiabática requiere el uso de una técnica iterativa.
a menos que se disponga de ecuaciones para los cambios de entalpía sensible de los productos de combustión
La temperatura de flama adiabática en proceso de combustión de de flujo estable se determina así
Q - W Hprod -Hreacc (1kJ>kmol combustible)
Establecer: Q=0
W=0
Produce: Hprod = Hreact
Una vez que se especifican los
reactivos y sus estados
El cálculo de la entalpía
de los productos Hprodu no es directo
Es fácil determinar la
entalpía de los reactivos Hreac
Biodiesel: cobra importancia por su valor ecológico
Tiene una gran ventaja
Reudcción de emeisiones
de Co2
Gracias al balance neutro de carbono
en la combustión
El combustible alternativo a Diesel es
el biodiesel obtenido de
restos de aceites comestibles
Grasas animales
Vegetales oleaginosos
se estudio de forma experimental
el comportamiento de un motor diésel
en una planta de generación de energía eléctrica
empleando el biodiesel obtenido apartir de aceite del piñón (Jatropha curcas) en diferentes porcentajes
Las mezclas que usaron del 20% y 30% de
biodiesel produjeron mayor potencia eléctrica
En cuanto al consumo horario de combustible se
obtuvo el mismo comportamiento.
Al incrementarse la potencia eléctrica,también
se incrementó el consumo del combustible
La opacidad generada por el motor de combustión interna de prueba.
Mostro una tendencia al incremento a medida que se incrementó la carga eléctrica
El torque generado en el motor de combustión interna al producirse la potencia eléctrica, tuvo un comportamiento lineal
Las densidades obtenidas de las diferentes mezclas, se
incrementaron levemente respecto al diésel
Lo cual le brinda una buena propiedad de lubricidad.
Poderes Caloríficos
la cantidad de energía desprendida en la reacción de combustión, referida a la unidad de masa de combustible.
La magnitud del poder calorífico puede
variar según como se mida.
Poder caolorífico inferior PCI
Es la cantidad total de calor desprendido
en la combustión completa de 1 kg de combustible
Sin contar la parte correspondiente al calor latente del vapor de agua de la combustión,
Poder calorífico superior PCS
Es la cantidad total de calor desprendido
en la combustión completa de 1 Kg de combustible
cuando el vapor de agua originado en la combustión está condensado y se contabiliza
Entalpía
Entapía de formación
Util para representar una sustancia en
un estado especificado debido a su composición química
Entalpía de combustión (hC)
Representa el calor liberado en la
combustión de flujo estable
cuando el combustible se quema
por completo a una T° y presión
especifica.
Expresada así : hR= hC= Hprod - H react
Entalpía de reacción (hR)
La diferencia entre
entalpía de los reactivos en el mismo
estado para una reacción completa
la entalpía de productos
en un estado específico
la cantidad de energía que el sistema absorbe
o libera en su entorno en procesos de presión constante
Existen diferentes tipos de energía como
Nuclear
vinculada a la estructura atómica
Química
Relativa a estructura molecular
En este caso se debe tener siempre
el estado de referencia
de la energía interna o entalpía de una
sustancia en ese estado
Ya que la composición final no es la
misma
Se conoce como: Estado de referencia estándar
Los valores se indican con el superíndice (°)
Como h° y u°
Por consiguiente en la combustión
Se rompen enlaces químicos existentes
Y se forman nuevos en las
moléculas.
Sensible y latente
Asociadas a cambio de estado
Reacción química
Donde se oxida combustible y libera energía
En el proceso de
Combustión
Si los componentes no quemados o quedan residuos
de combustible
El proceso es incompleto
Si todos los componentes del combustible se
queman en el proceso
La combustión es completa
No solo debe ponerse en contacto
proporciones iguales combustible y oxígeno
Para cuantificar estas
relaciones se emplea la AC
Relación aire-combustible
Se expresa en una
base de masa
Debe llevar alta su
Temperatura de ignición
Las mín. Aprox de varias sustancias del aire
atmosférico son de
Monóxido de carbono 610°C
Hidrógeno 580°C
Carbón 400°C
Gasolina 260°C
Hay dos componentes
importantes
Después de la reacción: Productos
Antes de la reacción: Reactivos
El O2 Puro
Se emplea como oxidante
En casos especiales
Soldadura
Corte
Oxidante más usado en esta reacción es el aire seco
Contiene aproximadamente 21 % de oxígeno - 79 % de nitrógeno en números molares.
Por consiguiente, cada mol de oxígeno que entra a una cámara de combustión será acompañado por 0.79/0.21 3.76 mol de nitrógeno
Nitrógeno
A T° muy elevadas el N2 reacciona con el O2
formando gases peligrosos
Sale a T° altas y absorbiendo
energía química.
Ingresa en gran cantidad en
la cámara de combustión y a baja T°
El aire seco está compuesto
pequeñas cantidades de dióxido de carbono, helio, neón e hidrógeno
0.9 % argón
78.1% de nitrógeno
por 20.9 % de oxígeno
Combustible
Combustibles alternativos
Su contenido energético por unidad de Vol
Es menor que
La gasolina o el Diesel
Combustiblrs de hidrocarburo son los derivados de
Hidrógeno Y Carbono
Ejemplos:
Alcohol metílico o metanol CH3OH
Diesel como dodecano C12h26
Gasolina como octano C8H18
Material que al quemarse genera energía