Nombre profesor: Matias Van Der Straten Waillet
Fecha: 31 de mayo de 2019
Curso: 1 medio b
Estudiante: Tomás García
La interacción entre elementos y moléculas conforman toda la materia y sus propiedades
El átomo es una partícula indivisible
PARTICULAS SUBATÓMICAS
Protones
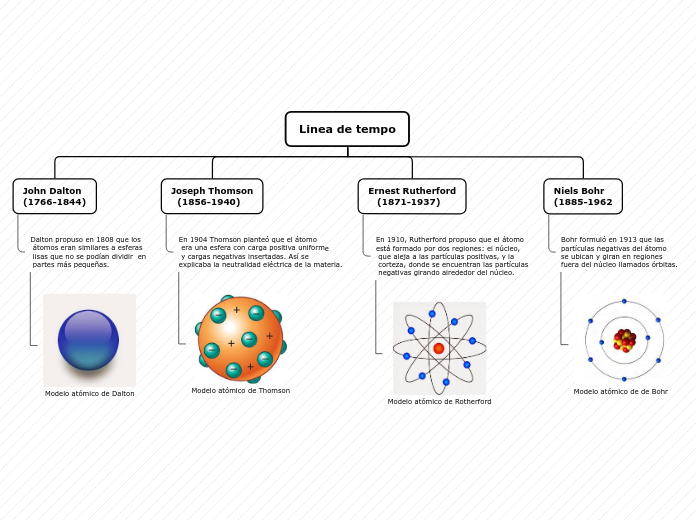
Ernest Rutherford
MODELO ATÓMICO DE BOHR
Niels Bohr
experimentos que lo condujeran a su modelo atómico
Los electrones siguen girando al rededor del núcleo, pero en niveles específicos, los cuales están cuantizados y permiten al electrón girar si perder o ganar energía.Si se le entrega energía al electrón, este puede saltar a un nivel superior
El modelo fisco–matemático sólo era capaz de hacer predicciones para el átomo de hidrogeno
MODELO ATÓMICO MECANOCUÁNTICO de Schrodinger
Erwin Schrodinger
un experimento que se formulo pero que nunca lo hizo, consistia en poner a un gato, una botella de veneno, y una maquina radioactiva con un 50% de desintegrarse en un tiempo determinado y liberar el venenop, por lo que la problbilidad de que el gato muera es equivalente y por esto no se sabe hasta abrir la caja si el gato esta muerto
que interpretando ésto mecanocuanticamente se encuentra en una superposicion de los estados posibles hasta que el observador intervenga.
Se basa en probabilidades de dónde se puede encontrar el electrón, en vez de este. Considera los ”cuantos” de Plank.
Tiene que haber un núcleo en el átomo en el cual se contiene la mayoría de la masa
Las partículas alfa se desviaban al pasar por la lamina de oro incluso hasta se devolvían
MODELO ATÓMICO DE RUTHERFORD
Electrones, con una pequeña masa y carga negativa el átomo debe ser neutro.El núcleo de átomo corresponde a protones con gran masa y carga positiva, y los electrones giran libremente alrededor del núcleo del átomo
que no pudo explicar la atracción entre nucleo y electrón porque decía que giraban libremente
Electrones
JJ Thomson
Como las cargas opuestas se atraen, entonces los rayos catódicos son negativos , que tal vez el rayo catódico es una partícula subatómica y que son particulas con masa
MODELO ATÓMICO THOMSON
Consiste en una partícula positiva, la cual usa todo el volumen del átomo
La distribución de la de la carga positiva en el interior de los átomos era errónea
el rayo catódico se acerca a los campos cargados positivamente y que el cambiar el material del cátodo no afectó al experimento
un tubo con un molinillo
que los rayos movían el molinillo
Demócrito