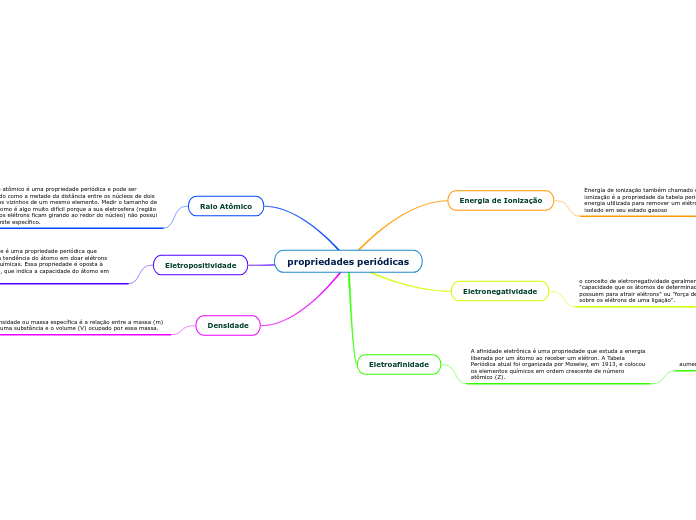
propriedades periódicas
Densidade
Densidade ou massa específica é a relação entre a massa (m) de uma substância e o volume (V) ocupado por essa massa.
A densidade é uma característica dos elementos químicos. A variação da densidade absoluta, no estado sólido, é uma propriedade periódica que aumenta de cima para baixo (vertical) e das extremidades para o centro (horizontal) na Tabela Periódica.
Eletropositividade
A eletropositividade é uma propriedade periódica que relaciona-se com a tendência do átomo em doar elétrons durante ligações químicas. Essa propriedade é oposta à eletronegatividade, que indica a capacidade do átomo em atrair os elétrons
A maioria dos elementos químicos eletropositivos são os metais alcalinos e os metais alcalinos terrosos, localizados, respectivamente, nas famílias IA e IIA da tabela periódica. Por esse motivo, a propriedade da eletropositividade também é chamada de caráter metálico.
Na medida que aumenta o números de camadas eletrônicas, é reduzida a força de atração do núcleo sobre os elétrons periféricos. Esse afastamento favorece a perda de elétrons pelo átomo e, em consequência disso, ele aumenta a sua eletropositividade.
Raio Atômico
O raio atômico é uma propriedade periódica e pode ser definido como a metade da distância entre os núcleos de dois átomos vizinhos de um mesmo elemento. Medir o tamanho de um átomo é algo muito difícil porque a sua eletrosfera (região onde os elétrons ficam girando ao redor do núcleo) não possui um limite específico.
Na tabela periódica, o raio atômico aumenta de cima para baixo na posição vertical. Já na horizontal, eles aumentam da direita para esquerda. O elemento químico que possui maior raio atômico é o Césio (Cs).
Eletroafinidade
A afinidade eletrônica é uma propriedade que estuda a energia liberada por um átomo ao receber um elétron. A Tabela Periódica atual foi organizada por Moseley, em 1913, e colocou os elementos químicos em ordem crescente de número atômico (Z).
aumenta de baixo pra cima da esquerda para a direita
Eletronegatividade
o conceito de eletronegatividade geralmente é definido como: "capacidade que os átomos de determinado elemento possuem para atrair elétrons" ou "força de atração exercida sobre os elétrons de uma ligação".
A maneira de saber sobre a eletronegatividade de um átomo é observando sua posição na Tabela Periódica, a Eletronegatividade cresce de baixo para cima e da esquerda para a direita.
Energia de Ionização
Energia de ionização também chamado de potencial de ionização é a propriedade da tabela periódica que indicará a energia utilizada para remover um elétron de um átomo isolado em seu estado gasoso
Para saber identificar o potencial de ionização basta observar a tabela periódica. É possível defini-la de acordo com a posição dos elementos químicos quanto a família ou ao período.
Então, a energia de ionização periódica é feita ao inverso do raio atômico. O raio atômico é de cima para baixo, da direita para a esquerda. O potencial de ionização é de baixo para cima e da esquerda para a direita.
2. No mesmo período: o potencial de ionização no mesmo período aumenta no sentido da esquerda para a direita. No mesmo período é quando os átomos tem quantidade igual de níveis. Ao tempo que os prótons aumentam, o nível de atração colocada sobre os elétrons também aumentam. Assim, é menor o raio atômico ao mesmo tempo que a energia de ionização aumenta.
1. Na mesma família: na mesma família, a energia de ionização aumenta no sentido de baixo para cima. Então, quando o elemento se encontra na mesma família, o tamanho do átomo aumenta ao mesmo tempo que aumenta os níveis ou camadas.