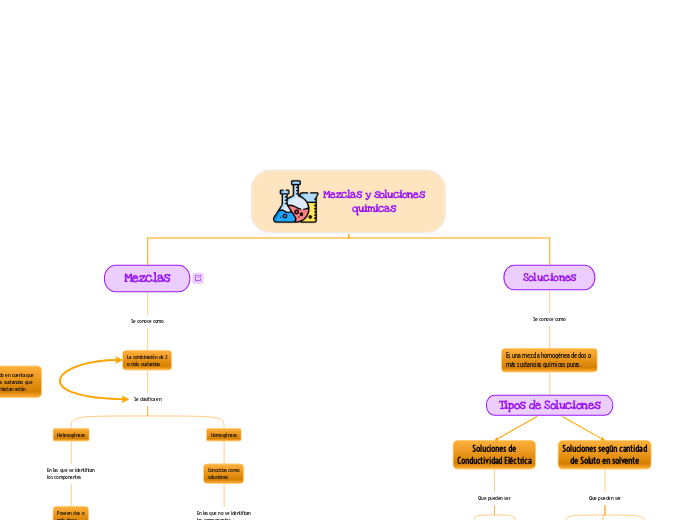
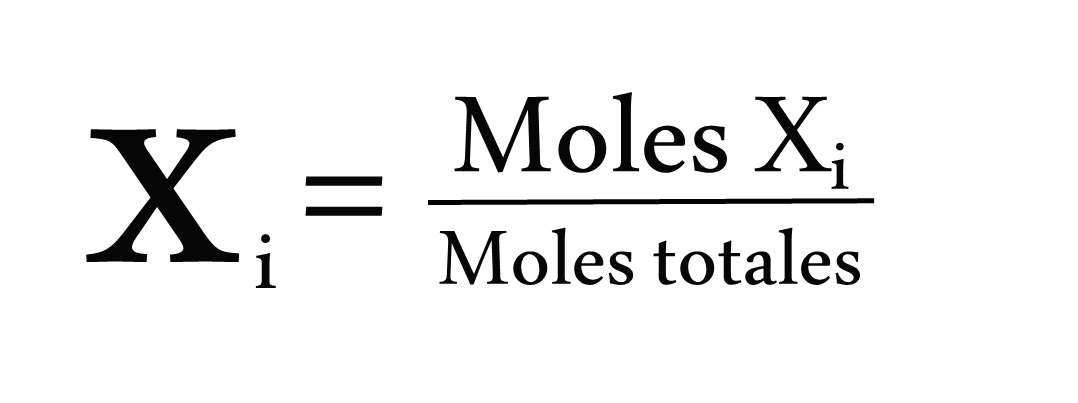Mezclas y soluciones
químicas
Mezclas
Se conoce como
La combinación de 2
o más sustancias
Se clasifica en
Heterogéneas
En las que se identifican
los componentes
Poseen dos o
más fases
Homogéneas
Conocidas como
soluciones
En las que no se identifican
los componentes
Poseen dos o
más fases
Tipos de mezclas
homogéneas
Subtopic
Suspensiones
Partículas >500nm
Coloides
Partículas entre 2 y 500nm
Soluciones
Partículas <2nm
Soluciones
Se conoce como
Es una mezcla homogénea de dos o
más sustancias químicas puras.
Tipos de Soluciones
Soluciones de
Conductividad Eléctrica
Que pueden ser
Soluciones
electrolíticas
Soluciones no
electrolíticas
Soluciones según cantidad
de Soluto en solvente
Que pueden ser
Soluciones
insaturadas
Soluciones
saturadas
Soluciones
sobre saturadas
Soluto
Sustancia de
menor proporción
Sustancias
disolventes
Sólido
Sustancia o
solutos a
disolver
Sólido
Ej: Bronce, aleaciones
Líquido
Ej: Amalgamas
Gaseoso
Ej: Hidrógeno en Platino
Líquido
Sustancia o
solutos a
disolver
Sólido
Ej: Agua de mar
Líquido
Ej: Licores
Gaseoso
Ej: Gaseosas
Gaseoso
Sustancia o
solutos a
disolver
Sólido
Ej: Humo, Smog
Líquido
Ej: Neblina
Gaseoso
Ej: Aire
Disolvente
Sustancia en
mayor proporción
Estas contienen
Sustancias
Llamadas
Soluto
Es la sustancia disuelta
Solvente
Es la sustancia que disuelve
Teniendo en cuenta que
hay dos sustancias que
contactan están
Las proporciones de
una respecto a otra se
conoce como
Concentración
Se puede expresar en
Términos cualitativos
como lo son
Insaturadas
Diluidas
Sobresaturadas
Concentradas
Términos cuantitativos
Estas a su vez
se dividen en
Unidades físicas
por ejemplo
Porcentaje masa-masa: %m/m

Porcentaje masa-volumen: %m/v

Porcentaje volumen-volumen: %v/v

Partes por millón: ppm

Partes por billón: ppb

Unidades químicas
Las cuales son
Molaridad
M
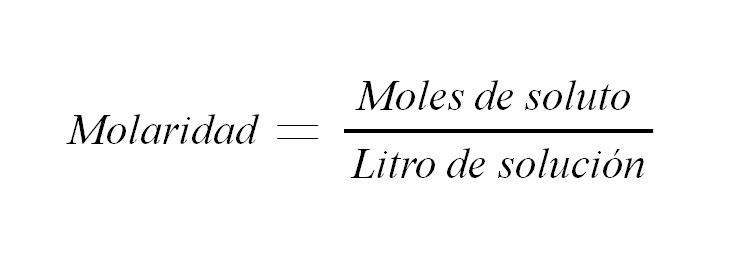
Normalidad
N

Molalidad
m

Fracción molar
Xsoluto/
Xsolvente