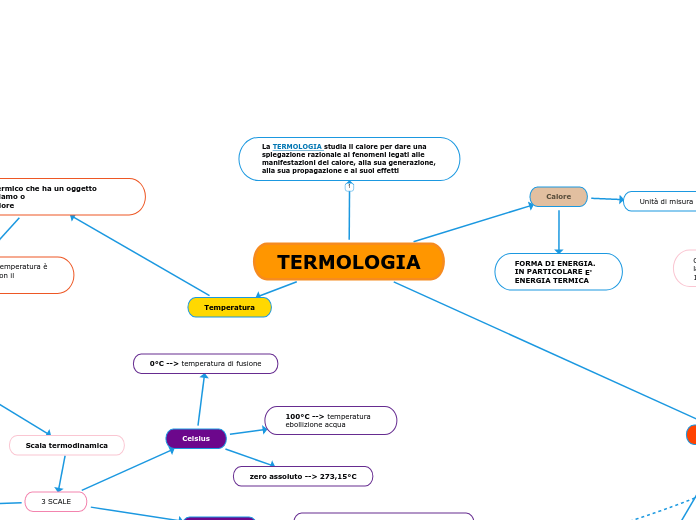
TERMOLOGIA
Temperatura
E’ il livello termico che ha un oggetto quando forniamo o
togliamo calore
DEFINIZIONE OPERATIVA --> La temperatura è la grandezza fisica che si misura con il TERMOMETRO
Calore
FORMA DI ENERGIA. IN PARTICOLARE E' ENERGIA TERMICA
Unità di misura
La TERMOLOGIA studia il calore per dare una spiegazione razionale ai fenomeni legati alle manifestazioni del calore, alla sua generazione, alla sua propagazione e ai suoi effetti
Teoria cinetica
Nei gas
Le molecole urtano contro le pareti del recipiente, ma gli urti sono elastici
Vqm = rad ( v12 + ... + v2N / N )
Le forze molecolari sono trascurabili
Il volume di ciascuna molecola è trascurabile rispetto all'intero volume
Ec = 3 / 2 R T
p = 1 / 3 d v2
Lavoro meccanico
Termometro
base del funzionamento
La DILATAZIONE TERMICA che subisce un liquido (alcol o mercurio)
DILATAZIONE TERMICA --> Fenomeno fisico che si realizza quando un corpo (liquido, gassoso o solido) aumenta di volume all'aumentare della temperatura
SOLIDI
Dilatazione volumica
ΔV = Vi α Δt
α = Coefficiente di dilatazione volumica
α = 3λ
LIQUIDI
COMPORTAMENTO ANOMALO DELL'ACQUA
Da 0°C a 4°C il suo volume, anzichè aumentare , diminuisce
GAS
TIPI
Da cucina
Ambientali
Clinici
Scala termodinamica
T(K)=T(°C) +273,15 T(°C) = T(K) -273,15
la temperatura MINIMA possibile teorica di un qualsiasi sistema termodinamico.
Gas perfetti
gas che soddisfa le...
Essi non esistono in natura. Sono oggetto di studio perché i gas reali si comportano con buona approssimazione come gas perfetti
Equazione di stato dei gas perfetti
p V = n R T
n = numero di moli
R --> Costante universale dei gas perfetti = 8,314 J / ( mol * k )
Dilatazione lineare
Δl = li λ Δt
λ = coefficiente di dilatazione lineare
LEGGI DEI GAS PERFETTI
legge di Boyle (isoterma)
Se la temperatura di una data massa di gas viene mantenuta costante, il volume V varia in modo inversamente proporzionale alla pressione p
leggi di Gay- lussac
prima legge (isobara)
A pressione costante Il volume del gas varia con una legge lineare espressa dalla formula ...
Vf = V0 (1 + α Δt)

GRAFICO --> Retta non passante per l'origine ( la relazione tra t e V è di tipo lineare)
seconda legge (isocora)
A volume costante, la pressione del gas varia con una legge lineare espressa dalla formula...
pt = p0 (1 + β Δt)

GRAFICO --> Retta non passante per l'origine ( la relazione tra t e p è di tipo lineare)
il calore ceduto da una parte del sistema è uguale al calore acquistato dall'altra
3 SCALE
Celsius
0°C --> temperatura di fusione
100°C --> temperatura ebollizione acqua
zero assoluto --> 273,15°C
Fahrenheit
32°F --> temperatura del ghiaccio
212°F --> temperatura ebollizione acqua
Kelvin (usata nel S.I.)
0 K = zero assoluto
273 k --> temperatura di fusione
373 k --> temperatura ebollizione acqua
Caloria (cal)
Quantità di calore necessaria per innalzare di 1°C la temperatura di 1 gr d'acqua distillata da 14,5°C a 15,5°C
1 cal = 4,186 J
Joule nel S.I.