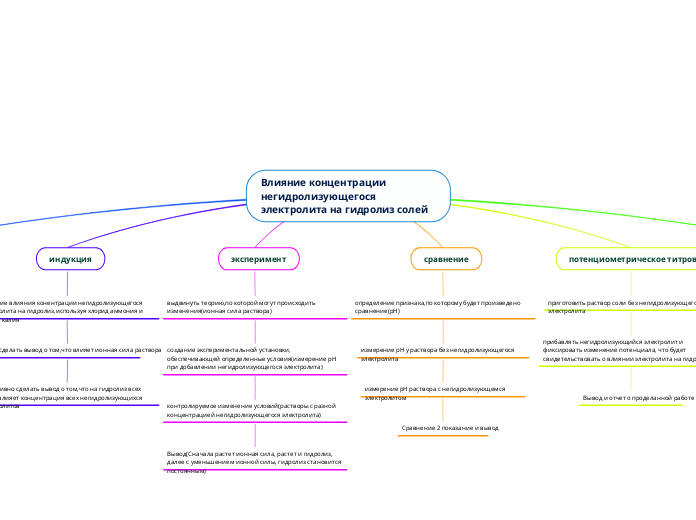
Влияние концентрации негидролизующегося электролита на гидролиз солей
химический анализ
изучение литературы и подборка методик по изучению негидролизующихся методик
выбор и проведение самой оптимальной методики анализа
вывод о влиянии концентрации негидролизующегося электролита на гидролиз солей
потенциометрическое титрование
приготовить раствор соли без негидролизующегося электролита
прибавлять негидролизующийся электролит и фиксировать изменение потенциала, что будет свидетельствовать о влиянии электролита на гидролиз
Вывод и отчет о проделанной работе
сравнение
определение признака,по которому будет произведено сравнение(pH)
измерение pH у раствора без негидролизующегося электролита
измерение pH раствора с негидролизующемся электролитом
Сравнение 2 показание и вывод
эксперимент
выдвинуть теорию,по которой могут происходить изменения(ионная сила раствора)
создание экспериментальной установки, обеспечивающей определенные условия(измерение pH при добавлении негидролизующегося электролита)
контролируемое изменение условий(растворы с разной концентрацией негидролизующегося электролита)
Вывод(Сначала растет ионная сила, растет и гидролиз, далее с уменьшением ионной силы, гидролиз становится постоянным)
индукция
изучение влияния конентрации негидролизующегося электролита на гидролиз,используя хлорид аммония и нитрат калия
сделать вывод о том,что влияет ионная сила раствора
индуктивно сделать вывод о том,что на гидролиз всех солей влияет концентрация всех негидролизующихся электролитов
Герменевтический
сбор информации о процессе гидролиза
изучение процесса гидролиза при изменении концентрации, определение взаимосвязи между концентрацией,константой гидролиза и ионной силой
формирование профессионального мнение о процессе гидролиза
объяснение влиянея концентрации негидролизующегося электролита на гидролиз(ионная сила)