Tienen diferente energía dependiendo la cercanía al núcleo
Las propiedades químicas son determinadas por los electrones que están fuera del núcleo
Representan el 99% de seres vivos
Se unen por enlaces covalentes llamados puentes de hidrogeno
Estos determinan muchas de las propiedades del agua
Calores específicos de vaporización y fusión
Alta tensión superficial
Gran Cohesión
Producción y propagación del impulso nervioso
(Ca+) son reconocidos como la contracción en los músculos
La molécula que se disuelve fácilmente en el agua se conoce como:
Hidrofilicas
A raíz de su polaridad, se excluyen activamente de la solución a las moléculas no polares
Las moléculas excluidas se conocen como:
Hidrofobicas
Los átomos del mismo elemento contienen diferentes números de neutrones
El peso atómico es protones + neutrones
Todos los elementos contienen el mismo número de protones
El número atómico es igual al número de protones en el núcleo
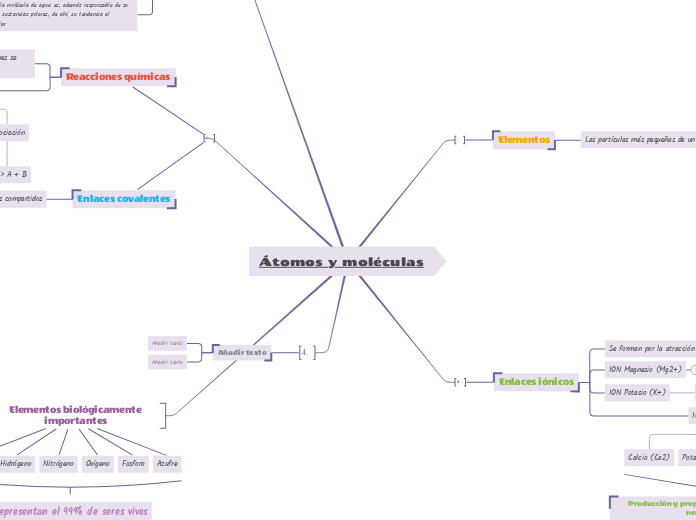
Átomos y moléculas
Elementos biológicamente importantes
Azufre
Fosforo
Oxígeno
Nitrógeno
Hidrógeno
Carbono
Añadir texto
Enlaces covalentes
Están formados por pares de electrones compartidos
Llamados orbital molecular
Envuelven a los núcleos de ambos átomos
Cada electrón pasa en su tiempo alrededor de un núcleo y el resto alrededor del otro
Complementan su nivel de energía y neutralizan la carga nuclear
Reacciones químicas
Tipos de reacción
Disociación
AB-> A + B
Combinación simple
A + B-> AB
De intercambio
AB + CD -> AD + CB
En enlace Covalente no polar los electrones se comparten por igual
El agua
La polaridad de la molécula de agua es, además responsable de su adhesión a otras sustancias polares, de ahí, su tendencia al movimiento capilar
La estructura del agua esta conformada por
Átomo de hidrogeno + átomo de oxígeno
Enlaces iónicos
IONES
Sodio (Na+)
Potasio (K+)
Calcio (Ca2)
ION Potasio (K+)
Con carga positiva en mayoría de los organismos
Se produce en los procesos biológicos
ION Magnesio (Mg2+)
Forma parte de una molécula clorofila
Consiste en atrapar energía radiante del sol
Se ve reflejado en algas y en plantas verdes
Se forman por la atracción mutua de partículas
Las sustancias iónicas pueden separarse fácilmente en agua
Dejando iones libres
De carga eléctrica opuesta
Siempre cuando un electrón salta de un átomo a otro