по Заводских Ярослав 10 месяца назад
127
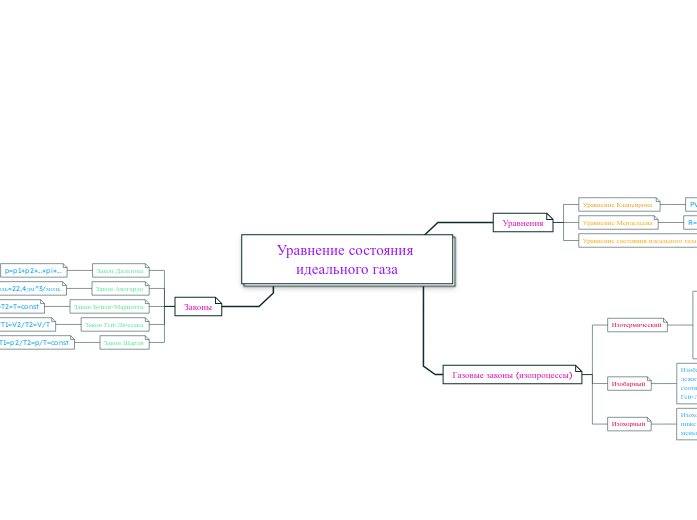
Уравнение состояния идеального газа
Уравнение состояния идеального газа описывает взаимосвязь между давлением, объемом и температурой газа. Основные уравнения включают уравнение Клапейрона и уравнение Менделеева-Клапейрона.