по Mafe Rubio 1 года назад
122
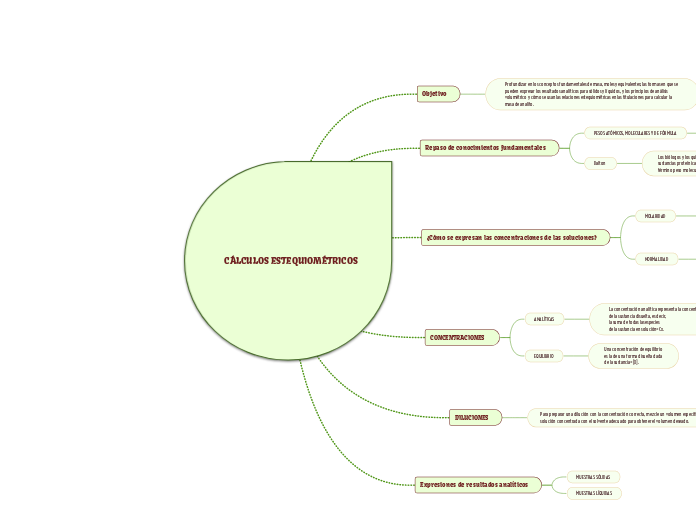
CÁLCULOS ESTEQUIOMÉTRICOS
En el ámbito de la química, es esencial comprender los conceptos fundamentales de masa, moles y equivalentes para una correcta interpretación de los resultados analíticos. Las muestras pueden ser tanto líquidas como sólidas, y los cálculos estequiométricos juegan un papel crucial en el análisis volumétrico.