по LADY CAROLINA REYES LOPEZ 4 лет назад
228
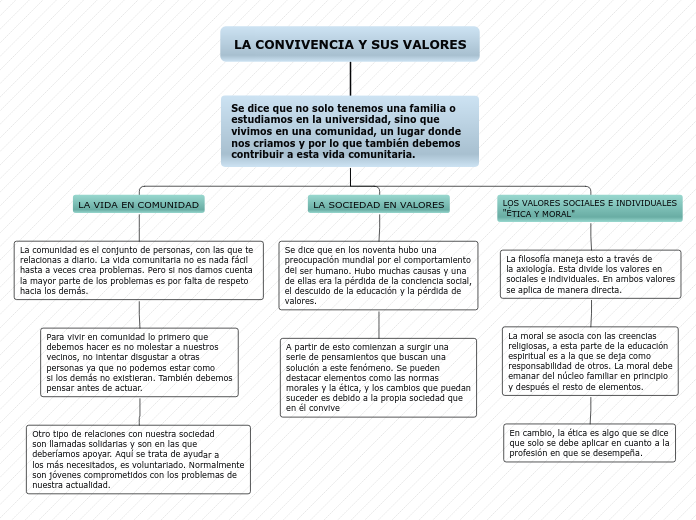
Organigrama arbol
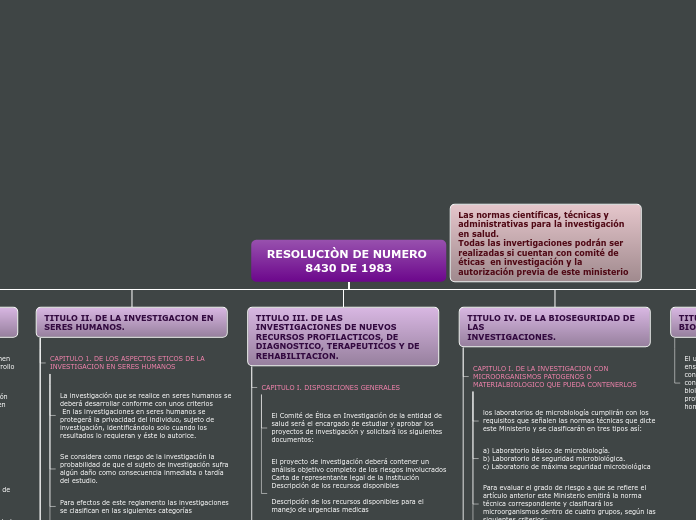
Este documento regula la investigación en seres humanos, estableciendo criterios éticos y de privacidad para proteger a los sujetos de estudio. Las investigaciones se clasifican según el nivel de riesgo: