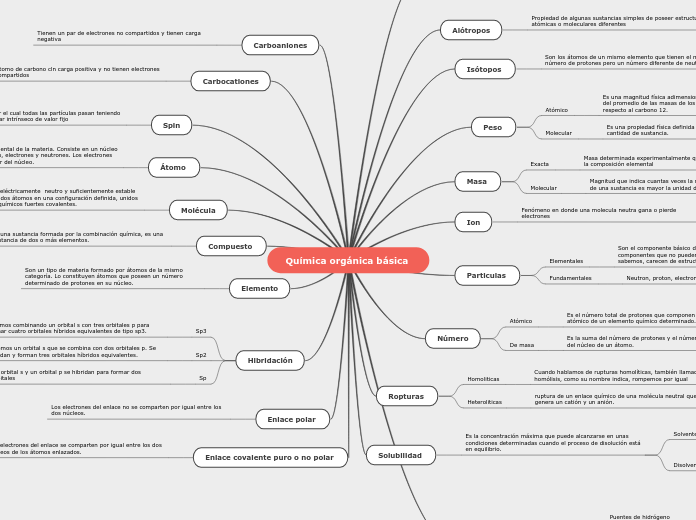
Química orgánica básica
Enlace covalente puro o no polar
Los electrones del enlace se comparten por igual entre los dos núcleos de los átomos enlazados.
Enlace polar
Los electrones del enlace no se comparten por igual entre los dos núcleos.
Hibridación
Sp
Un orbital s y un orbital p se hibridan para formar dos orbitales
Sp2
Tenemos un orbital s que se combina con dos orbitales p. Se hibridan y forman tres orbitales híbridos equivalentes.
Sp3
Estamos combinando un orbital s con tres orbitales p para formar cuatro orbitales híbridos equivalentes de tipo sp3.
Elemento
Son un tipo de materia formado por átomos de la mismo categoría. Lo constituyen átomos que poseen un número determinado de protones en su núcleo.
Compuesto
Es una sustancia formada por la combinación química, es una sustancia de dos o más elementos.
Molécula
Es un grupo eléctricamente neutro y suficientemente estable de al menos dos átomos en una configuración definida, unidos por enlaces químicos fuertes covalentes.
Átomo
Es la unidad fundamental de la materia. Consiste en un núcleo redondo de protones, electrones y neutrones. Los electrones se mueven alrededor del núcleo.
Spin
Propiedad física por el cual todas las partículas pasan teniendo un momento angular intrínseco de valor fijo
Carbocationes
Un átomo de carbono cln carga positiva y no tienen electrones no compartidos
Carboaniones
Tienen un par de electrones no compartidos y tienen carga negativa
Fuerzas intermoleculares
ion-dipolo
Un ion unido a un dipolo. Tienen una carga formal positiva/negativa unida con una parcial positiva/ negativa
Dipolo-dipolo
Consiste en dos cargas, una negativa y una positiva, separadas por una distancia dada
Puentes de hidrógeno
cuando un átomo de hidrógeno unido a un átomo fuertemente electronegativo existe en las proximidades de otro átomo electronegativo con un par solitario de electrones.
Solubilidad
Es la concentración máxima que puede alcanzarse en unas condiciones determinadas cuando el proceso de disolución está en equilibrio.
Disolventes
No polares
Disuelven a moleculas no polares( dependiendo de lo que más le convenga).
Polares
Disuelven a moleculas polares
Solventes
Sustancia química que me permite separar moleculas
Ropturas
Heteroliticas
ruptura de un enlace químico de una molécula neutral que genera un catión y un anión.
Homoliticas
Cuando hablamos de rupturas homolíticas, también llamada homólisis, como su nombre indica, rompemos por igual
Número
De masa
Es la suma del número de protones y el número de neutrones del núcleo de un átomo.
Es el número total de protones que componen el núcleo atómico de un elemento químico determinado.
Particulas
Fundamentales
Neutron, proton, electron
Elementales
Son el componente básico de la materia, es decir aquellos componentes que no pueden dividirse más y que, por lo que sabemos, carecen de estructura interna.
Ion
Fenómeno en donde una molecula neutra gana o pierde electrones
Masa
Molecular
Magnitud que indica cuantas veces la masa de una molécula de una sustancia es mayor la unidad de masa atómica
Exacta
Masa determinada experimentalmente que permite determinar la composición elemental
Peso
Molecular
Es una propiedad física definida como su masa por unidad de cantidad de sustancia.
Atómico
Es una magnitud física adimensional, definido como la razón del promedio de las masas de los átomos de un elemento con respecto al carbono 12.
Isótopos
Son los átomos de un mismo elemento que tienen el mismo número de protones pero un número diferente de neutrones
Alótropos
Propiedad de algunas sustancias simples de poseer estructuras atómicas o moleculares diferentes
Radicales libres
Tienen un electrón no compartido y son neutros