av Katherin Caza för 4 årar sedan
663
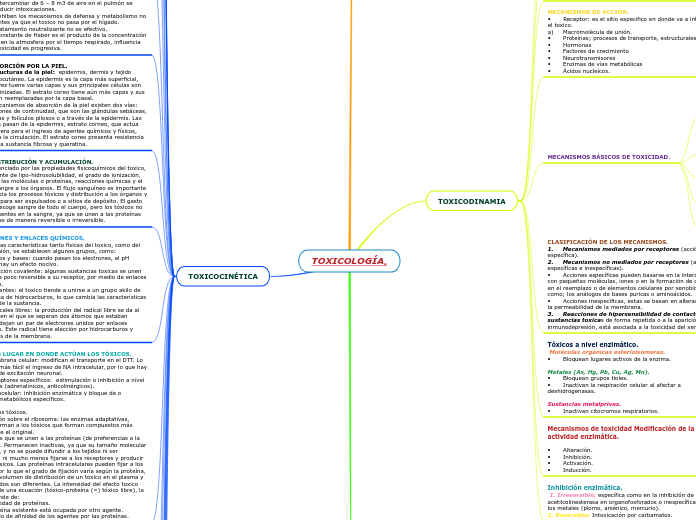
TOXICOLOGÍA.
En el campo de la toxicología, uno de los procesos esenciales es la toxicocinética, que se refiere a cómo un tóxico se oxida y se elimina del cuerpo. La oxidación de los tóxicos implica una serie de reacciones químicas, donde el NADPH se oxida a NADP, transfiriendo un hidrógeno a una flavoproteína.