Enlaces químicos y propiedades
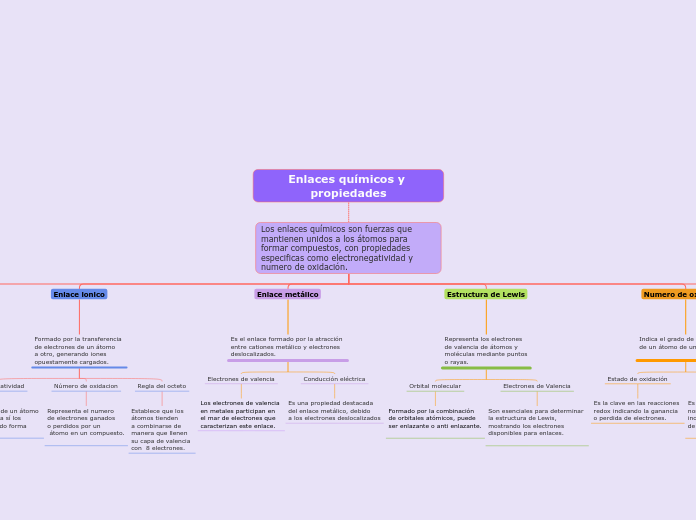
Los enlaces químicos son fuerzas que mantienen unidos a los átomos para formar compuestos, con propiedades especificas como electronegatividad y numero de oxidación.
Guía la formación de enlaces covalentes
Excepciones
Algunos elementos pueden
no seguir esta regla debido
a su configuración electrónica
particular.
Estabilidad molecular
Átomos que buscan completar
su capa de valencia para
alcanzar estabilidad.
Numero de oxidación
Indica el grado de oxidación
de un átomo de un compuesto
Determinación
Es fundamental en la
nomenclatura de compuestos
inorgánicos y en el balanceo
de ecuaciones químicas.
Estado de oxidación
Es la clave en las reacciones
redox indicando la ganancia
o perdida de electrones.
Estructura de Lewis
Representa los electrones
de valencia de átomos y
moléculas mediante puntos
o rayas.
Electrones de Valencia
Son esenciales para determinar
la estructura de Lewis,
mostrando los electrones
disponibles para enlaces.
Orbital molecular
Formado por la combinación
de orbitales atómicos, puede
ser enlazante o anti enlazante.
Enlace metálico
Es el enlace formado por la atracción
entre cationes metálico y electrones
deslocalizados.
Conducción eléctrica
Es una propiedad destacada
del enlace metálico, debido
a los electrones deslocalizados
Los electrones de valencia
en metales participan en
el mar de electrones que
caracterizan este enlace.
Enlace ionico
Formado por la transferencia
de electrones de un átomo
a otro, generando iones
opuestamente cargados.
Regla del octeto
Establece que los
átomos tienden
a combinarse de
manera que llenen
su capa de valencia
con 8 electrones.
Número de oxidacion
Representa el numero
de electrones ganados
o perdidos por un
átomo en un compuesto.
Electronegatividad
Es la capacidad de un átomo
para atraer hacia sí los
electrones cuando forma
un compuesto.
Enlace covalente
Es un tipo de enlace donde los
átomos comparten uno o mas
pares de electrones
Electrones antienlazantes
Electrones que ocupan
orbitales moleculares
anti enlazantes, disminuyendo
la estabilidad del enlace.
Eletrones enlazantes
Son los electrones
compartidos entre
átomos en un enlace
covalente.
Electrones de valencia
Son aquellos electrones en
la capa externa del átomo
que participan en el enlace.