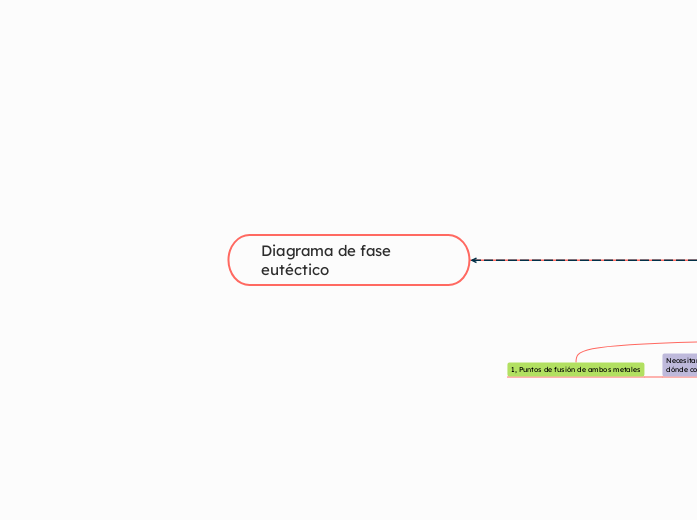
Diagrama de fase eutéctico
Propiedades de metales:
Puntos de fusión, solubilidad, estructuras cristalinas.
Diagramas experimentales existentes:
Busca diagramas de sistemas similares para referencia.
Reglas de Gibbs y diagramas de equilibrio:
Entender cómo las fases cambian con la temperatura y la composición.
Interpretación de diagramas binarios:
4. Definir el tipo de sistema
Dos metales completamente solubles en estado líquido y parcialmente solubles en sólido
Se mezclan completamente en estado líquido, pero forman fases α y β en estado sólido.
Ejemplo: Ag-Cu.
Diagrama típico: Similar al eutéctico, pero con zonas adicionales donde las fases α y β coexisten parcialmente.
Dos metales completamente solubles en estado sólido
Forman una solución sólida continua (una única fase sólida).
Ejemplo: Cu-Ni.
Diagrama típico: Liquidos y solidos forman curvas suaves sin punto eutéctico, solo transición de líquido a sólido.
Dos metales completamente insolubles en estado sólido
Forman fases separadas α y β en estado sólido.
Ejemplo: Pb-Sn.
Diagrama típico: Curvas de liquidos descendiendo hacia el punto eutéctico y solidos formando una línea horizontal en Te.
6. Determina qué fases están presentes en cada zona del diagrama.
Fase sólida (α + β o solución sólida)
Por debajo de solidos
Zona mixta (L + α, L + β)
Entre liquidos y solidos
Zona líquida (L)
Por encima de liquidos
5. Dibujar el diagrama de fase
Identificar fases
Determina qué fases están presentes en cada zona del diagrama.
Dibujar curvas
Liquidus: Curvas que indican el inicio de la solidificación.
Solidus: Líneas donde termina la solidificación.
Colocar puntos importantes
Punto de fusión de A y B en los extremos.
Punto eutéctico (si aplica).
Establecer ejes
Eje X: Composición (% de A y B).
Eje Y: Temperatura (°C o K).
3. Composición eutéctica y temperatura eutéctica
Es fundamental conocer el porcentaje de composición donde ocurre el punto eutéctico y la temperatura correspondiente.
2. Comportamiento de solubilidad:
En estado sólido:
¿Son completamente solubles, insolubles o parcialmente solubles?
En estado líquido:
¿Forman una solución líquida completa o parcial?
1, Puntos de fusión de ambos metales
Necesitarás las temperaturas de fusión para saber dónde colocar los extremos del diagrama