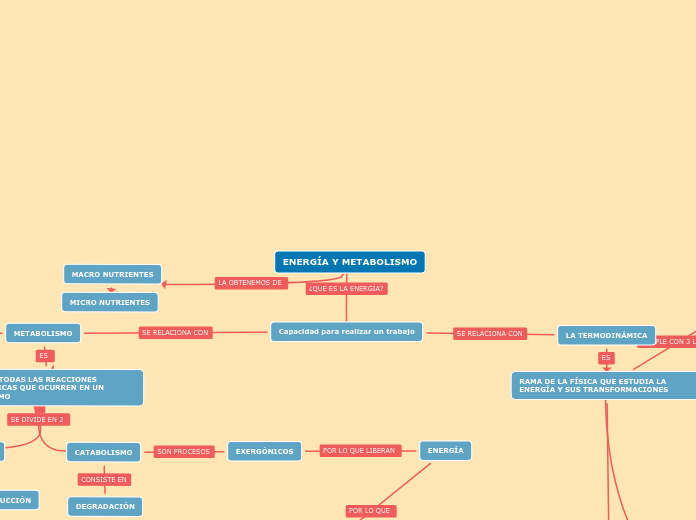
ENERGÍA Y METABOLISMO
MACRO NUTRIENTES
MICRO NUTRIENTES
Capacidad para realizar un trabajo
LA TERMODINÁMICA
RAMA DE LA FÍSICA QUE ESTUDIA LA ENERGÍA Y SUS TRANSFORMACIONES
3RA LEY
LA ENTROPIA DE CUALQUIER SISTEMA A 0K ES IGUAL A 0
HABRÁ MÁXIMO ORDEN
2DA LEY
TODOS LOS PROCESOS FÍSICOS Y QUIMICOS SOLO SE PRODUCEN ESPONTÁNEAMENTE CUANDO AUMENTA EL DESORDEN.
ENTROPIA
ENERGIA LIBRE DE GIBSS (G)
UNA FUNCIÓN DE ESTADO
LA ESPONTANEIDAD DE UN PROCESO
NO ESPONTANEO
SE REQUIERE UN APORTE DE ENERGÍA PARA MANTENER UN CAMBIO
G > 0
ESPONTANEO
SE PRODUCEN CAMBIOS FÍSICOS O QUÍMICOS CON LIBERACIÓN DE ENERGÍA
G< 0
MEDIR EL GRADO DE DESORDEN DE UN SISTEMA
1ERA LEY
LA ENERGÍA NO PUEDE CREARSE NI DESTRUIRSE
ENERGÍA INTERNA (E)
ENTALPIA (H)
SI UNA REACCION ES EXOTERMICA
DESPRENDE CALOR
H < O
ENDOTERMICA
ABSORBE CALOR
H > 0
MEDIDA DE CALOR GANADO O PERDIDO, ESTA RELACIONADO A LA ENERGÍA REQUERIDA PARA ROMPER ENLACES QUÍMICOS
LA CANTIDAD TOTAL DE ENERGÍA EN UN SISTEMA Y SU ENTORNO
E= CALOR (q) + TRABAJO (w)
METABOLISMO
Adquisición y utilización de energía
Síntesis de moléculas necesarias para la estructura de las células
Eliminación de productos de desecho
SUMA DE TODAS LAS REACCIONES BIOQUÍMICAS QUE OCURREN EN UN ORGANISMO
CATABOLISMO
EXERGÓNICOS
PRODUCEN
DEGRADACIÓN
MACROLÉCULAS
MOLÉCULAS MAS SIMPLES
ANABOLISMO
ENDERGÓNIGOS
ENERGÍA
CONSUMEN
ATP
3 GRUPOS FOSFATO
1 AZÚCAR DE 5 CARBONOS (PENTOSA) LLAMADA RIBOSA
1 BASE NITROGENADA DE 2 ANILLOS LLAMADA ADENINA
Subtopic
ADENOSIN TRIFOSTAFO
MOLÉCULA DONDE SE CONSERVA LA ENERGÍA
BIOSINTESIS O CONSTRUCCIÓN
MACROMOLÉCULAS
MOLÉCULAS MAS PEQUEÑAS