por Gael Hernadez Vargas hace 3 años
276
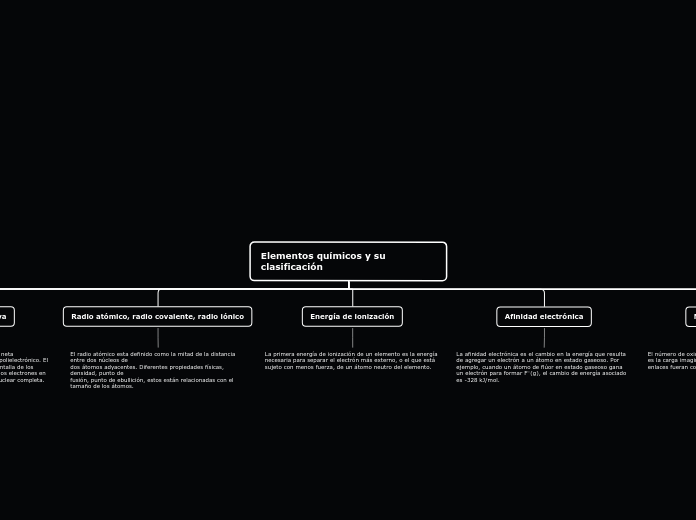
Elementos químicos y su clasificación
La corteza terrestre está compuesta predominantemente por ocho elementos químicos, entre los que destacan el oxígeno y el silicio. Estos elementos forman el 98,5 % de la corteza, mientras que el resto de los elementos apenas representan el 1,5 %