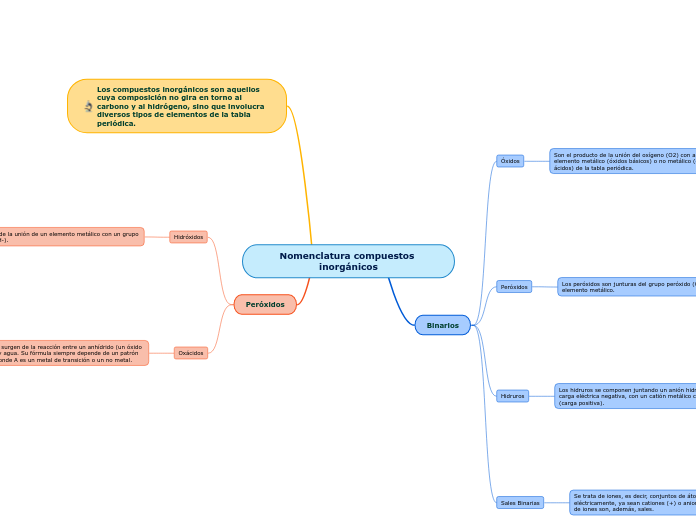
Nomenclatura compuestos inorgánicos
Oxácidos
Ácidos que surgen de la reacción entre un anhídrido (un óxido no metal) y agua. Su fórmula siempre depende de un patrón HaAbOc, donde A es un metal de transición o un no metal.
SISTEMÁTICA: Comienza con el prefijo que indica el número de oxígenos seguido de la palabra “oxo” seguido del prefijo que indica el número de átomos del elemento no metálico, y la raíz del elemento no metálico acabado en “ato”, en números romanos indicamos la valencia del elemento no metálico. Finalmente añadimos por último las palabras «de hidrógeno«.
EJEMPLOS: H3AsO3 Trioxoarseniato (III) de Hidrogeno
HCLO2 Dioxoclorado (III) de Hidrogeno
STOCK: Comienza con la palabra ácido , seguido del prefijo que indica el número de oxígenos más la palabra “oxo” y por último el prefijo que indica el número de átomos del elemento no metálico (generalmente 1) seguido de la raíz del elemento no metálico terminado en “ico” y en números romanos indicamos su valencia.
EJEMLPOS: H3AsO3 Acido Trioxoarsenico (III)
HCLO2 Acido Dioxoclorico (III)
TRADICIONAL: se nombra con la palabra ácido seguido de la raíz del elemento no metálico e indicando la valencia con la que actúa según el siguiente criterio.
EJEMPLOS: H3AsO3 Acido Arsenioso
HCLO2 Acido cloroso
Hidróxidos
Resultantes de la unión de un elemento metálico con un grupo hidroxilo (OH-).
SISTEMÁTICA: Se anteponen los prefijos numéricos a la palabra hidróxido.
EJEMPLOS: Mg(OH)2 Dihidroxido de Mgnesio
AuOH Monohidroxido de oro
STOCK: En esta nomenclatura se comienza con la palabra hidróxido seguido del elemento metálico, en donde la valencia del mismo se expresará en números romanos y entre paréntesis.
EJEMPLOS: Mg(OH) Hidroxido de Magnesio(II)
AuOH Hidroxido de Oro
TRADICIONAL: Esta nomenclatura comienza con la palabra hidróxido seguido del elemento, siempre teniendo en cuenta la valencia con la que actúa.
EJEMPLOS: Mg(OH)2 Hidroxido Magnesico
AuOH Hidroxido Auroso
Los compuestos inorgánicos son aquellos cuya composición no gira en torno al carbono y al hidrógeno, sino que involucra diversos tipos de elementos de la tabla periódica.
Binarios
Sales Binarias
Se trata de iones, es decir, conjuntos de átomos cargados eléctricamente, ya sean cationes (+) o aniones (-). Este tipo de iones son, además, sales.
EJEMPLOS: CaBr2 Dibromuro de Calcio
CoF2 Difluoruro de Cobalto.
STOCK:
Se realiza indicando el número de valencia del elemento metálico entre paréntesis y en números romanos, precedido por la expresión “…-uro de”+ elemento metálico.
EJEMPLOS: CaBr2 Bromuro de Calcio
CoF2 Fluoruro de Cobalto (II)
TRADICIONAL:
Se realiza nombrando el elemento no metálico terminado en – uro seguido del elemento metálico. Se debe de tener en cuenta la valencia del elemento metálico.
EJEMPLOS: CaBr2 Bromuro Calcico
CoF2 Fluoruro Cobaltoso
Hidruros
Los hidruros se componen juntando un anión hidruro (H-) de carga eléctrica negativa, con un catión metálico cualquiera (carga positiva).
SISTEMATICA:
Se indica mediante un prefijo el número de átomos de cada elemento.
EJEMPLOS:CaH2 Dihidruro de Calcio
CoH2 Dihidruro de cobalto
STOCK:
Se realiza indicando el número de valencia del elemento metálico entre paréntesis y en números romanos, precedido por la expresión “hidruro de”+ elemento metálico.
Ejemplos: CaH2 Hidruro de Calcio
CoH2 Hidruro de Cobalto (II)
TRADICIONAL: Se nombra con la palabra hidruro seguido del elemento metálico.
EJEMPLOS: CaH2 Hidruro Calcico
CoH2 Hidruro Cobaltoso
Peróxidos
Los peróxidos son junturas del grupo peróxido (O2-2) con un elemento metálico.
SISTEMATICA:
Se indica mediante un prefijo el número de átomos de cada elemento.Los prefijos utilizados que indican el número de átomos en esta nomenclatura son:
EJEMPLOS:CuO2 Dióxido de cobre.
PbO4 Tetraóxido de plomo.
STOCK:
Se realiza indicando el número de valencia del elemento metálico entre paréntesis y en números romanos, precedido por la expresión «peróxido de» + elemento metálico.
EJEMPLOS: Na2O2 Peroxido de Sodio
Ti2(O2)3 Peroxido de titanio (III)
TRADICIONAL: Se nombra con la palabra peróxido seguida del elemento metálico y su respectivo prefijo teniendo en cuenta la valencia del elemento metálico.
EJEMPLOS: CuO2 Peróxido cúprico.
PbO4 Peróxido plúmbico.
Óxidos
Son el producto de la unión del oxígeno (O2) con algún elemento metálico (óxidos básicos) o no metálico (óxidos ácidos) de la tabla periódica.
Nomenclatura
Tradicional:
En esta forma de nomenclatura consideramos sufijos prefijos que dependen de la cantidad de valencias que tenga el elemento con el que se forma el óxido.
EJEMPLOS:CrO Óxido hipocromoso
Cr2O3 Óxido cromoso
STOCK:
Se utiliza el término óxido, pero no se le sin ningún prefijo, después se sitúa la partícula "de" y a continuación de pone el nombre del elemento, seguido, si es necesario, de su valencia en números romanos.
EJEMPLOS:Fe2O3 Óxido de hierro (III)
FeO Oxido de hierro (II)
SISTEMATICA:
Se utiliza el término óxido precedido de el prefijo numérico que le corresponde al oxigeno, para el elemento, su nombre precedido tambien por el prefijo numérico que le corresponde, unidos los 2 elementos por la particula "de".
EJEMPLOS: Fe2O3 Trioxido de dihierro.
FeO Óxido de hierro