da IRLANDA DIAZ LEAL mancano 5 anni
1485
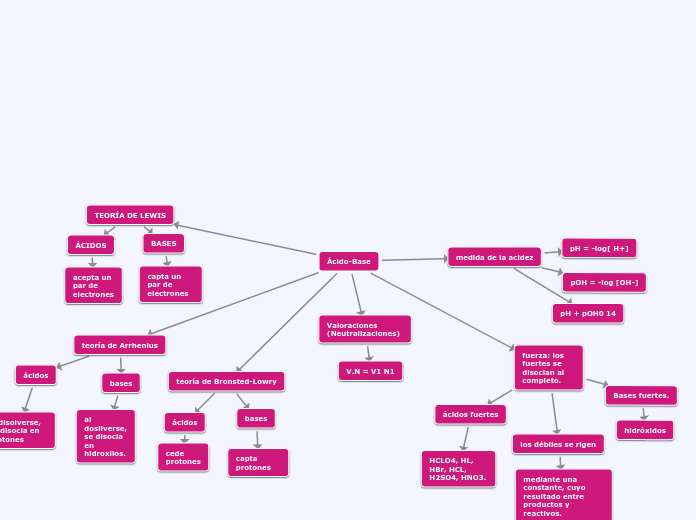
mapa acido base
En la química, las teorías de ácido-base son fundamentales para entender las reacciones químicas. La teoría de Lewis describe los ácidos como sustancias que aceptan un par de electrones y las bases como aquellas que donan un par de electrones.