INTEGRIDAD Y MOVILIDAD ARTICULAR
CAPACIDAD AEROBICA
CIRCULACIÓN
Estrés adaptativo
Hipertrofia ventricular de tipo concéntrico
Disfunción diastólica
Alteración en la capacidad del ventrículo para relajarse y llenarse adecuadamente
Menor distensibilidad ventricular
Disminución de la FEVI
Disminución del flujo sanguíneo a órganos y tejidos
Disfunción sistólica
Reducción en la capacidad del ventrículo de contracción y eyección
Disfunción beta adrenérgica
Inhibe el factor de crecimiento endotelial vascular
Disminución de transmisión de impulsos eléctricos
Bradicardia asociada a quimioterapia
Disminución de síntesis de óxido nítrico en las arteriolas
Vasoconstricción
HTA
Liberación de radicales libres
Inflamación miocárdica
Alteración en la homeostasis del hierro
Conversión de hierro ferroso a férrico
Destrucción de las membranas mitocondriales, nucleares, la membrana celular y del retículo endoplásmico
fibrosis por quimioterapia
Descenso del calcio intracelular
Disminución de la contractibilidad
Neurotoxicidad
Postura antiálgica
Predominio flexor
Modificaciones biomecánicas posturales
Línea funcional posterior en bloqueo largo
POSTURA
Disminución de la fuerza y sinergia de m. posturales
Alteración en el sistema postural
Alteración del control selectivo de MII
Modificaciones
Estrategias de movimiento
APAS ineficientes
Menores estrategias de control postural
Tobillo
Desalineamiento de punto claves central y pélvico
Cintura pélvica
Afectación de la locomoción
Fase de balanceo
Alteración de parámetros
Temporales
Menor velocidad
Aumento de la demanda energética
Patrón ineficiente
MARCHA
Menor periodo de paso
Menor periodo de balanceo
Menor cadencia
Espaciales
Aumento del ancho de paso
Aumento del ángulo de paso
Diminución de la longitud de paso
Disminución de la longitud de zancada
Fase de apoyo
Menores reacciones de enderezamiento
BALANCE
Paso
Cadera
Control dinámico
Ineficiente alineación corporal
Deterioro del equilibrio estático y dinámico
Dificultad para realizar transferencias y cambios de posición
MOVILIDAD Y LOCOMOCIÓN
Restricciones biomecánicas
Disminución grados de libertad
RANGO DE MOVIMIENTO
Orientación espacial
Desplazamiento del CG
Alteración límites de verticalidad
Glúteo mayor
Dorsal ancho
Línea anterior superficial bloqueo corto
Triángulo femoral
Pectineo
Psoas
Recto femoral
Esternocleidomastoideo
Línea posterior superficial bloqueo largo
Erector de la columna
DOLOR
Cabeza adelantada y en flexión de cuello
Protrusión de hombros
Aumento de la cifosis dorsal
Disminución de la lordosis lumbar
Retroversión pélvica
Ganglio de la raíz dorsal
Fibras tipo C
Médula espinal asta posterior
Asta sensitiva
Laminas de Rexed (I, II, V)
Se decusa
Tracto espinotalámico lateral
Tálamo
Condiciones degenerativas sistematizadas
Dying back
Patrón específico de daño neuronal
Axones de las neuronas periféricas sufren daño
Degeneración desde la terminal del axón hacia el soma
Respuesta tras exposición a químicos neurotóxicos
Alteración del metabolismo nervioso
Alteración del transporte axonal
Disminución de la conducción nerviosa
Disfunción mitocondrial
Reduce la energía disponible para el mantenimiento del axón y la vaina de mielina
Degeneración axonal
Aumenta de la producción de especies reactivas de oxígeno (ROS)
Repercusión en la mitocondria
Daño en membranas axonales
Degeneración distal
Cambios en el metabolismo muscular, afectando la capacidad de los músculos para metabolizar el lactato eficientemente
Acumulación de lactato en los tejidos musculares
Inmunosupresión de linfocitos T y macrófagos
Ambiente celular acido
Afección en la función y la supervivencia de las células satélite
Reducción de la capacidad de reparación
Favorecimiento de la invasión tumoral
Neuropatía periférica inducida por quimioterapia (NPIQ)
Dolor neuropático
Disfunción nerviosa
Reducción en la velocidad de conducción de los impulsos nerviosos.
Conducción nerviosa ineficaz
Disminuye la capacidad de las neuronas motoras para comunicar señales efectivas
Afectación en la unión neuromuscular
No se genera adecuado potencial de acción
Inadecuada liberación de acetilcolina (ACh)
No se une a los receptores de acetilcolina en el sarcolema
No se da la apertura de canales iónicos
iones de Na+ no entran en la célula
No se despolariza la membrana
No hay reclutamiento de los túbulos transversos
No hay liberación de Ca2+ desde el retículo sarcoplásmico
NO se une el Ca2+ a la troponina
Ineficiente ciclo de puentes cruzados
Ineficiente contracción muscular
Alteración en la fuerza, resistencia y potencia muscular
DESEMPEÑO MUSCULAR
INTEGRIDAD DE NERVIO CRANEAL Y PERIFERICO
Fenómenos inmunomediados
alteraciones en la expresión de canales iónicos
daño en el ADN mitocondrial
disrupción en el transporte axonal por funcionamiento anormal de los microtúbulos
Complicación neurológica más frecuente relacionada con la quimioterapia
Hiperactividad del receptor RANK/RANK–L
Reducción de la capacidad del sistema inmunológico para reconocer y eliminar las células malignas
Inducción de células T reguladoras
Inhibición de actividad de las células T citotóxicas
Producción de citoquinas inmunosupresoras
Instauración en médula ósea
Modificación del microambiente medular
Secreción de factores que suprimen la respuesta inmune local
Alteración de la expresión de moléculas de presentación de antígenos
Cambios en la matriz extracelular
Alteración en el remodelado óseo
Aumento de los factores de activación de osteoclastos
Mayor actividad osteoclástica
Activación del Dickkopf1 (DKK-1)
Papel fisiopatológico en la disminución de la masa ósea
Disminución de la actividad osteoblástica
Disminución de la densidad mineral ósea
Imbalance entre la producción y resorción ósea
Liberación de grandes cantidades de calcio al torrente sanguíneo
Osteolisis
Múltiples lesiones líticas
Movilización sustancial del calcio del hueso
Hipercalcemia
Acumulación de proteínas plasmáticas anormales
Afecta la comunicación celular
Promoción de un ambiente que favorezca supervivencia celular
Desarrollo de mecanismos que les permiten evadir la apoptosis
Producción de metaloproteinasas de matriz (MMPs)
Degradación
Altera el soporte estructural del tejido
Facilita la migración y diseminación de las células malignas
Alteración en células del estroma
Secreción de factores angiogénicos
Activación del factor de crecimiento endotelial vascular
Producción de citoquinas pro inflamatorias
Liberación de histamina
ILK 2
Factor de necrosis tumoral (TNF-α)
inflamación crónica
Sensibilización de los nociceptores
Afecta la señalización celular necesaria para la regeneración muscular
Factor inibidor de los macrógafos
Linfotoxina
ILK 1
ILK 6
Múltiples focos de tumoración
MIELOMA MÚLTIPLE (C900)
Modificación en el proceso de glucólisis
Glucosa no se convierte en piruvato
No se transporta a las mitocondrias para su metabolismo aeróbico
Efecto Warburg
Piruvato se convierte en lactato
Acúmulo de lactato en sangre
Disminución en la eliminación de lactato
Hiperlactatemia
Producto principal del metabolismo anaeróbico aumentado en las células tumorales
No ingresa al ciclo de Krebs
Microambiente hipóxico debido a vascularización inadecuada
Lactato como subproducto
Complicación metabólica de las neoplasias hematológicas
Acidosis láctica
Lesiones líticas en cabeza femoral izquierda, ilíaco izquierdo
Modificación de los planos articulares
Alteración en la artrocinematica de la art cadera
INTEGRIDAD ESQUELÉTICA
Perfil monoclonal con presencia de banda IgG de patrón oligoclonal Kappa y Lambda
Menor volumen óseo trabecular en cuerpo vertebral de S1
Disminución de la resistencia a fuerzas compresivas
Modificación en densidad ósea
Aumento de riesgo de fractura patológica
Formación de tumor a nivel de columna
RMN de columna lumbosacra que reporta masa sacra entre S1 y S2
Compresión en canal central de predominio izquierdo
Estenosis
Desplazamiento a agujero sacro derecho y ala sacra derecha
Transplante autólogo de MO
Junio 2024
Requerimiento de tratamiento con quimioterapia
Inflamación y fibrosis en los tejidos irradiados
Medicamentos citostáticos
Citotoxicidad
Inhiben la neoplasia
Actúan sobre la médula ósea
Daño en. células hematopoyéticas
Inhibición de su capacidad de proliferación
Disminución de la eritropoyesis
Menor producción de glóbulos rojos
Disminución de la Hb
Menor consumo y transporte de oxígeno
Mielotoxicidad
Supresión de la producción celular en la médula ósea
Neutropenia
Trombocitopenia
Anemia
Interferencia en la división celular
Interferencia en la formación y función del huso mitótico
Impedimento de la separación adecuada de los cromosomas durante la mitosis
Apoptosis
Detenimiento de la división celular
4 ciclos comprendidos entre febrero-mayo 2024
Aproximadamente un 50% de los POS desarrollan un MM
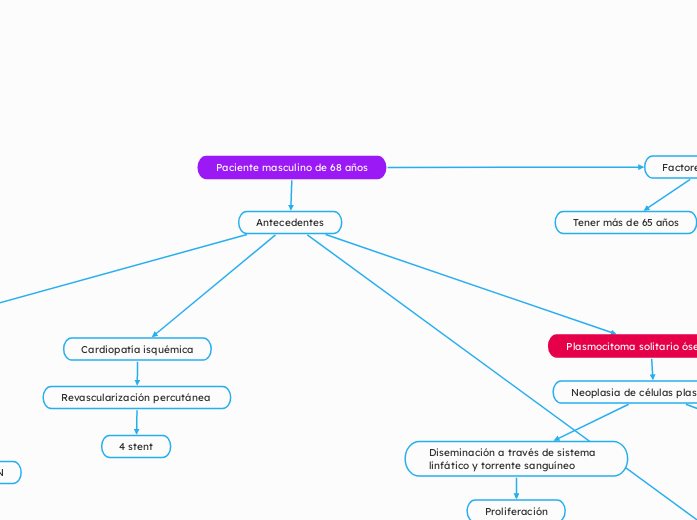
Paciente masculino de 68 años
Factores de riesgo
Tener más de 65 años
Mieloma múltiple es más prevalente en hombres
Antecedentes
Plasmocitoma solitario óseo (POS)
Antecedentes de radioterapia (2022)
Neoplasia de células plasmáticas
Diseminación a través de sistema linfático y torrente sanguíneo
Proliferación
Secreción de factores de crecimiento y citoquinas
Fagocitosis de linfocitos T
Aumento de supervivencia
Tumor localizado
Lesión lítica solitaria de células plasmáticas
Predominio en columna vertebral
Cardiopatía isquémica
Revascularización percutánea
4 stent
Diabetes mellitus tipo 2
hiperglucemia crónica
Daño a lípidos, proteínas y ADN
reducción de la capacidad antioxidante
Estrés oxidativo
Daño neuronal
Aumento de la producción de radicales libres de oxígeno