by Kellys Carreño rangel 4 years ago
397
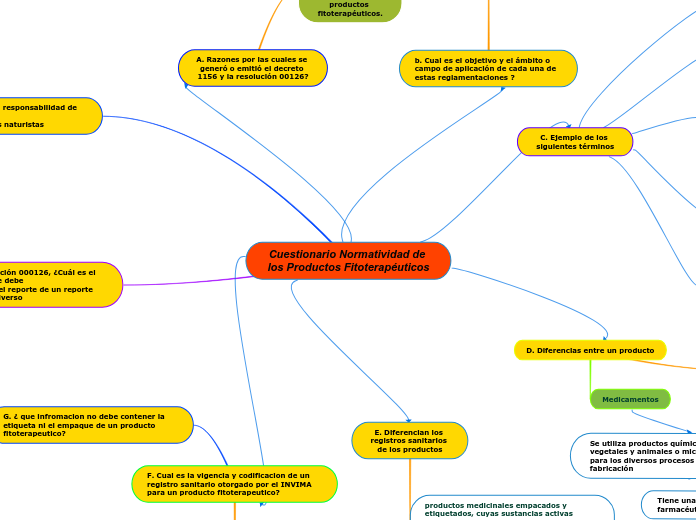
Cuestionario Normatividad de los Productos Fitoterapéuticos
La regulación de productos fitoterapéuticos busca estandarizar y simplificar el registro sanitario conforme a las normas internacionales. Los productos fitoterapéuticos son aquellos que contienen sustancias activas derivadas de plantas medicinales y han sido modificados químicamente, físicamente o biológicamente.