av Катерина Комарова 4 år siden
561
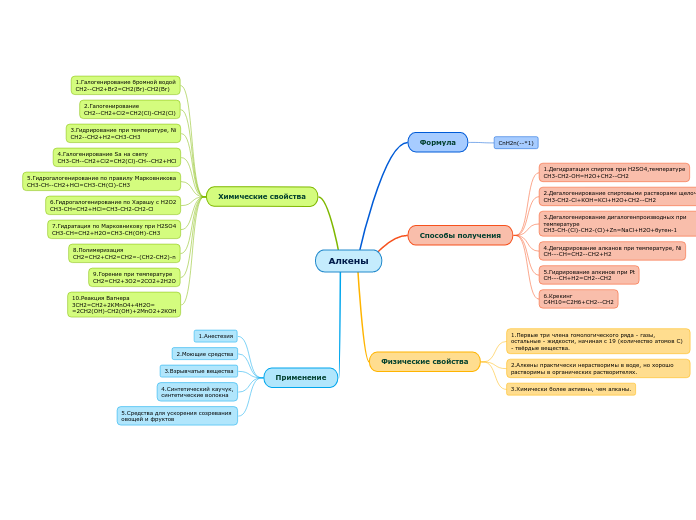
Алкены
Алкены представляют собой важный класс органических соединений, отличающихся наличием двойной связи между атомами углерода. Физические свойства алкенов зависят от их молекулярной массы:
av Катерина Комарова 4 år siden
561

Mer som dette