av Adnan Miranda Padilla 2 måneder siden
28
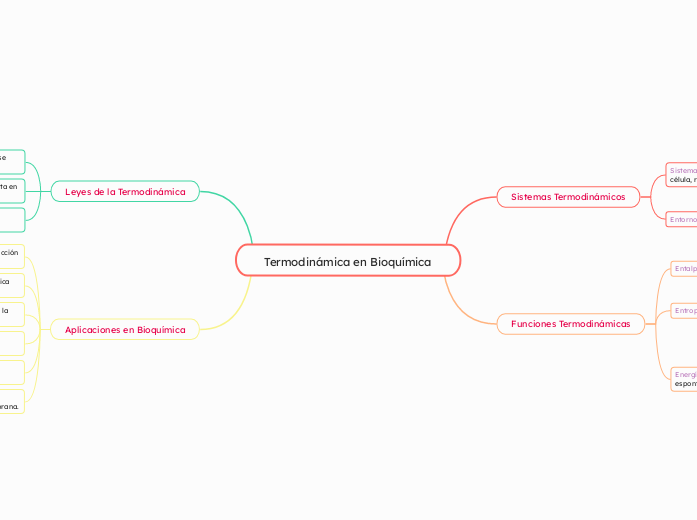
Termodinámica en Bioquímica
La termodinámica en bioquímica se centra en el estudio de los sistemas y su interacción con el entorno, categorizados en cerrados, abiertos y aislados según su capacidad para intercambiar energía y materia.