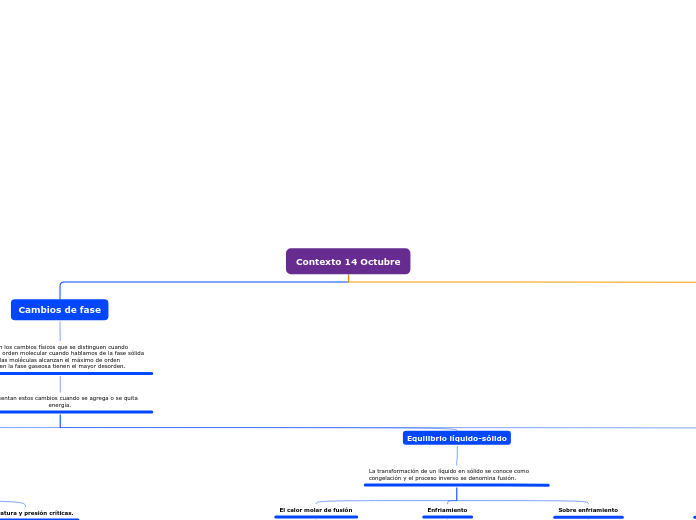
Contexto 14 Octubre
Diagrama de Fases
Resume las condiciones en las cuales una sustancia existe como sólido, líquido o gas.
Anticipan las direcciones de las transiciones de las fases producidas por los cambios de temperatura y presión
Estos permiten predecir los cambios en el punto de fusión y en el punto de ebullición de una sustancia debido a los cambios de la presión externa.
Cambios de fase
Son los cambios físicos que se distinguen cuando
cambia el orden molecular cuando hablamos de la fase sólida las moléculas alcanzan el máximo de orden
y en la fase gaseosa tienen el mayor desorden.
Se presentan estos cambios cuando se agrega o se quita energía.
Equilibrio sólido-vapor
Deposición
Las moléculas hacen la
transición directa de vapor a sólido
Sublimación
Es el proceso en el cual las moléculas pasan directamente de sólido a vapor.
Equilibrio líquido-sólido
La transformación de un líquido en sólido se conoce como congelación y el proceso inverso se denomina fusión.
Sobre enfriamiento
Un líquido se puede enfriar temporalmente por debajo de su punto de congelación.
Enfriamiento
Su temperatura disminuye.
El calor molar de fusión
Es la energía necesaria para fundir un mol de un sólido.
Equilibrio líquido-vapor.
Calor molar de vaporización y punto de ebullición
Temperatura y presión críticas.
Presión críticas.
Es la presión mínima que se debe aplicar para llevar a cabo la licuefacción a la
temperatura crítica.
Temperatura críticas
Es temperatura más alta a la cual una sustancia puede existir en forma líquida.
Punto de ebullición
Es la temperatura en la cual la presión de vapor de un líquido es igual a la presión externa. En el se forman burbujas dentro de liquido.
Este es una medida de la intensidad de las fuerzas
intermoleculares que se ejercen en un líquido. Esta propiedad se puede definir como la energía, la cual es necesaria para evaporar un mol de un líquido.
Presión de vapor
Cuando un líquido se evapora, sus moléculas gaseosas ejercen este vapor.
La evaporación es el proceso en el cual un
líquido se transforma en gas.