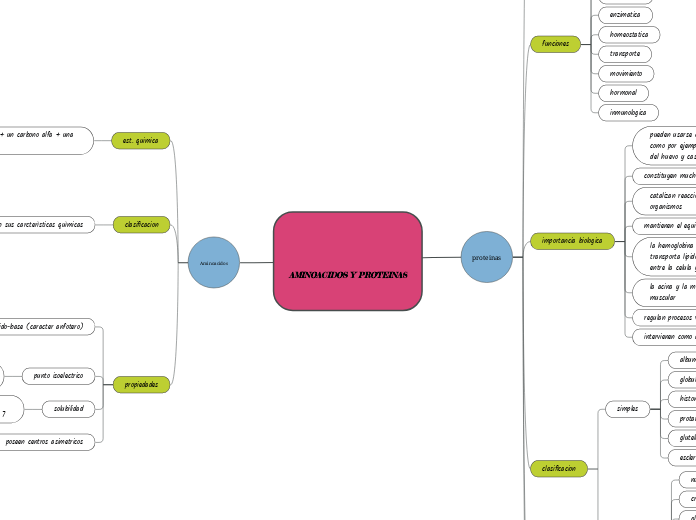
AMINOACIDOS Y PROTEINAS
Aminoacidos
poseen centros asimetricos
poseen carbono quiral, por lo tanto van a ser levogiros o dextrogiros, dependiendo de que lado este el grupo amino
solubilidad
La solubilidad de los aminoácidos se mide calculando la variación de Energía Libre en contacto con agua a pH = 7
punto isoelectrico
es al PH en el cual cada aminoacido se encuentra neutro entre sus cargas
acido-base (caracter anfotero)
A PH bajo, mayor concentraciòn de H+, el aa capta H+ y queda con carga (+). A PH alto, menor concentraciòn de H+, el aa cede H+ y queda con carga (-). A PH=7 el aa es neutro. Es decir dependiendo el ph pueden actuar como acidos o bases
segùn sus carcterìsticas quìmicas
grupo 4: AA polares bàsicos: tienen màs de un grupo amino
grupo 3: AA polares acidos: tienen màs de un grupo carboxilo
grupo2: AA polares no ionizables: el resto R con cadenas hidrocarbonadas cortas, en las que hay funciones polares (alcohol, tiol, amida)
grupo 1: AA apolares: al tener largas cadenas hidrocarbonadas R no posee cargas electricas
est. quimica
formadas por un grupo carboxilo + un carbono alfa + una funciòn amino
proteinas
desnaturalizacion y renaturalizacion
la segunda puede existir excepto cuando el agente causante de la desnaturalizacion es el calor
la primera se puede dar debido a cambios de ph, tª, etc y es la perdida parcial o total de los niveles de estructura superiores al primario
propiedades
especifidad de funcion: cada proteina tiene un funcion en concreto diferente.
solubilidad: las macromoleculas solubles en agua no forman disoluciones sino dispersiones coloidales
clasificacion
conjugadas
metaloproteinas
lipoproteinas
fosfoproteinas
glicoproteinas
cromoproteinas
nucleoproteinas
simples
escleroproteinas
glutelinas y aliadinas
protaminas
histonas
globulinas
albuminas
importancia biologica
intervienen como defensa frente a agentes patogenos
regulan procesos vitales (insulina)
la acina y la mioctina son responsables de la contraccion muscular
la hemoglobina transporta oxigeno, la seroalbumina transporta lipidos y la permeasas producen el intercambio entre la celula y el exterior
mantienen el equilibrio osmotico del medio
catalizan reacciones metabolicas que se producen en los organismos
constituyen muchas membranas de los seres vivos
pueden usarse con un fin energetico en casos especiales como por ejemplo el desarrollo embrionario (ovoalbumina del huevo y caseinas de la leche)
funciones
inmunologica
hormonal
movimiento
transporte
homeostatica
enzimatica
estructural
de reserva
estructura
macromoleculas formadas a partir de la polimnerizacion de aa, unidos gracias a el enlace de tipo amida entre ellos y la consiguiente formacion de estructuras
est. terciaria: plegamjiento y se combinanacion de las laminas beta y las alfa helice formando motivos, tomando forma de proteina globular o fibrosa. Y se le añaden otras fuerzas como vander walls, puentes disulfuro, etc
estas estructuras se dan gracias al enlace peptidico entre los aminoacidos (entre el grupo carboxilo de una molecula con el amino de la siguiente, y la liberacion de una molecula de h2o)
est. secudnaria: disposicion espacial mantenida mediante puentes de hidrogeno, en forma alfa hèlice o beta plegamiento
est. primaria: dada por la organizacion, numero e identidad de cada AA