Referencias:
Rubio, S., Pacheco-Orozco, R. A., Gómez, A. M., Perdomo, S., & García-Robles, R. (2020). Secuenciación de nueva generación (NGS) de ADN: presente y futuro en la práctica clínica. Universitas Medica, 61(2). https://doi.org/10.11144/javeriana.umed61-2.sngs
guilar-Bultet, Lisandra, & Falquet, Laurent. (2015). Secuenciación y ensamblaje de novo de genomas bacterianos: una alternativa para el estudio de nuevos patógenos. Revista de Salud Animal, 37(2), 125-132. Recuperado en 21 de mayo de 2024, de http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0253-570X2015000200008&lng=es&tlng=es.
Klug, W., Cumming, M., & Spencer, C. (2006). Conceptos de
Genética. Madrid: PEARSON Prentice Hall.
Colaboradores, Oficina de Prensa y. «La metabolómica como una herramienta en la
investigación». Centro de Investigación en Alimentación y Desarrollo (CIAD), 12 de octubre de
2023, https://www.ciad.mx/la-metabolomica-como-una-herramienta-en-la-investigacion/.
De Les Illes Balears, U. (n.d.). Cromatografía de gases. Área De Cromatografia - Instrumentos, Servicios Y Equipos - Servicios Cientificotécnicos - Universitat De Les Illes Balears. https://sct.uib.es/Instruments-i-equips-dels-Serveis-Cientificotecnics/Area-de-cromatografia/Cromatografia-de-gases.cid108074
Tamay de Dios, L., Ibarra, C., & Velasquillo, C. (2013). Fundamentos de la reacción en cadena de la polimerasa (PCR) y de la PCR en tiempo real. Investigación en discapacidad, 2(2), 70-78.
Iglesias Bueno, J. J. (2021). Análisis bioinformático de expresión génica diferencial en tomate.
Castellanos, L., González, L. J., & Padrón, G. INTRODUCCIÓN. ALGUNOS CONCEPTOS BÁSICOS.
transcriptómica. (n.d.). Autoridad Europea De Seguridad Alimentaria. https://www.efsa.europa.eu/es/glossary/transcriptomics
Tecnología de microarrays (chips de ADN o ARN). (n.d.). Genome.gov. https://www.genome.gov/es/genetics-glossary/Tecnologia-de-microarrays
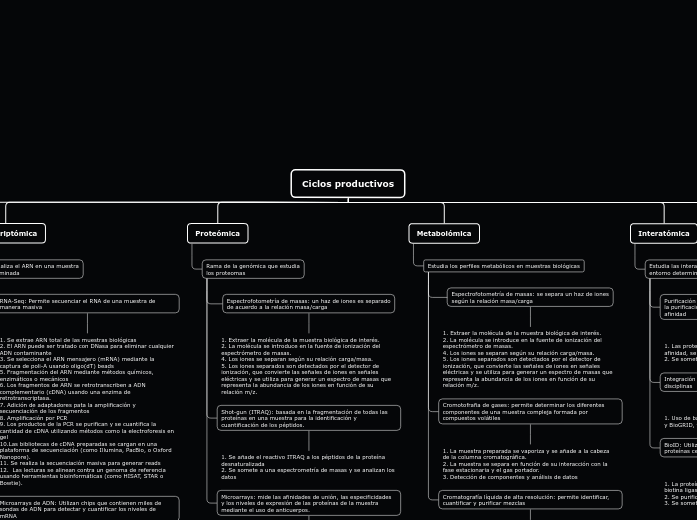
Ciclos productivos
Alimentómica
Estudia los alimentos y su interacción con el humano
1. Se utiliza un chip que contiene miles de genes representados en pequeñas áreas específicas.
2. El ARNm se toma de dos muestras para comparar.
3. Se generan dos sondas marcadas diferencialmente con diferentes fluorocromos, como Cy3 y Cy5.
3. Las sondas apuntan a secuencias de genes complementarios en el chip
4. Un escáner como el Agilent G2565CA mide la intensidad de la fluorescencia
Interatómica
Estudia las interacciones entre distintas biomoléculas en un entorno determinado
BioID: Utiliza una enzima modificada que biotinila las proteínas cercanas a la proteína de interés.
1. La proteína de interés se fusiona con una enzima como la biotina ligasa.
2. Se purifican con estreptavidina.
3. Se someten a espectrofotometría de masas.
Integración de Datos Ómicos: Combina datos de diversas disciplinas
1. Uso de bases de datos de interacción como STRING, IntAct y BioGRID, y software de análisis de redes como Cytoscape.
Purificación por Afinidad y espectrometría de masas: combina la purificación de complejos proteicos mediante etiquetas de afinidad
1. Las proteínas de interés se marcan con una etiqueta de afinidad, se purifican junto con sus proteínas asociadas
2. Se someten a una espectrofotometría de masas
Metabolómica
Estudia los perfiles metabólicos en muestras biológicas
Cromatografía líquida de alta resolución: permite identificar, cuantificar y purificar mezclas
1. Los componentes de la muestra se disuelven en un cartucho y se añaden al cabezal de la columna cromatográfica.
2.Los componentes de la muestra pasan a través de la columna cromatográfica gracias a la presión.
3. Se analizan los datos y la detección de componentes.
Cromotofrafia de gases: permite determinar los diferentes componentes de una muestra compleja formada por compuestos volátiles
1. La muestra preparada se vaporiza y se añade a la cabeza de la columna cromatográfica.
2. La muestra se separa en función de su interacción con la fase estacionaria y el gas portador.
3. Detección de componentes y análisis de datos
Espectrofotometría de masas: se separa un haz de iones
según la relación masa/carga
Proteómica
Rama de la genómica que estudia
los proteomas
Microarrays: mide las afinidades de unión, las especificidades y los niveles de expresión de las proteínas de la muestra mediante el uso de anticuerpos.
1. Colocar las proteínas seleccionadas o sus anticuerpos al chip
2. Se extraen las proteínas y se marcan
3. Se añaden al chip para su complementación
4. Un escáner como el Agilent G2565CA mide la intensidad de la fluorescencia
5. Se analizan los datos
Shot-gun (ITRAQ): basada en la fragmentación de todas las proteínas en una muestra para la identificación y cuantificación de los péptidos.
1. Se añade el reactivo ITRAQ a los péptidos de la proteína desnaturalizada
2. Se somete a una espectrometría de masas y se analizan los datos
Espectrofotometría de masas: un haz de iones es separado
de acuerdo a la relación masa/carga
1. Extraer la molécula de la muestra biológica de interés.
2. La molécula se introduce en la fuente de ionización del espectrómetro de masas.
4. Los iones se separan según su relación carga/masa.
5. Los iones separados son detectados por el detector de ionización, que convierte las señales de iones en señales eléctricas y se utiliza para generar un espectro de masas que representa la abundancia de los iones en función de su relación m/z.
Transcriptómica
Se analiza el ARN en una muestra
determinada
qPCR: Se utiliza para detectar y cuantificar secuencias de ácidos nucleicos específicas mediante el uso de indicadores fluorescentes en la reacción.
1. Extraiga el ARN total de muestras biológicas utilizando kits de extracción comerciales y trate el ARN con ADNasa para eliminar cualquier ADN contaminante.
2. Cuantificar el ARN utilizando un espectrofotómetro
3. Evaluar la calidad del ARN mediante electroforesis en gel.
4. síntesis de ADNc
5. Reparación de mezcla de qPCR
6. Cargue la mezcla de qPCR en una placa de PCR en un ciclador térmico.
7. Después de pasar por los cicladores y medir la
fluorescencia y los datos se analizan
Microarrays de ADN: Utilizan chips que contienen miles de sondas de ADN para detectar y cuantificar los niveles de mRNA
1. Utiliza un chip que contiene miles de genes representados en pequeñas áreas específicas.
2. El ARNm se toma de dos muestras para comparar.
3. Se generan dos sondas marcadas diferencialmente con diferentes fluorocromos, como Cy3 y Cy5.
3. Se añaden sondas a secuencias de genes complementarios en el chip.
4. Un escáner como el Agilent G2565CA mide la intensidad de la fluorescencia
5. La fluorescencia en cada sonda indica la presencia y cantidad del ARNm correspondiente en la muestra.
RNA-Seq: Permite secuenciar el RNA de una muestra de manera masiva
1. Se extrae ARN total de las muestras biológicas
2. El ARN puede ser tratado con DNasa para eliminar cualquier ADN contaminante
3. Se selecciona el ARN mensajero (mRNA) mediante la captura de poli-A usando oligo(dT) beads
5. Fragmentación del ARN mediante métodos químicos, enzimáticos o mecánicos
6. Los fragmentos de ARN se retrotranscriben a ADN complementario (cDNA) usando una enzima de retrotranscriptasa.
7. Adición de adaptadores pata la amplificación y secuenciación de los fragmentos
8. Amplificación por PCR
9. Los productos de la PCR se purifican y se cuantifica la cantidad de cDNA utilizando métodos como la electroforesis en gel
10.Las bibliotecas de cDNA preparadas se cargan en una plataforma de secuenciación (como Illumina, PacBio, o Oxford Nanopore).
11. Se realiza la secuenciación masiva para generar reads
12. Las lecturas se alinean contra un genoma de referencia usando herramientas bioinformáticas (como HISAT, STAR o Bowtie).
Genómica
Estudio completo de los genomas
Microarrays de ADN: Se colocan secuencias de ADN
en un chip donde se unen a las secuencias
del chip que produce una reacción de luz
1. Se utiliza un chip que contiene miles de genes representados en pequeñas áreas específicas.
2. Se toma el mRNA de dos muestras a comparar
3. Se generan dos sondas marcadas diferencialmente con fluorocromos diferentes, como Cy3 y Cy5
3. Las sondas se a las secuencias de genes complementarios en el chip
4. Un escaner como el Agilent G2565CA mide la intensidad de la fluorescencia
Ensamblaje de genomas: Desarrollar una secuenciacion mediante fragmentos de ADN complementando
con bioinformatica.
1. Corroborar la calidad de los datos
2. Se identifican todos los pares de reads que se solapan lo suficientemente bien
3. Se calculan los solapamientos entre los reads para determinar cuáles tienen secuencias iguales
4. Construcción del gráfico de solapamientos llamado Layout
5. Se utilizan algoritmos de ensamblaje que aprovechan la estructura del gráfico que corresponden a segmentos del genoma que están siendo ensamblados
6. Se verifica la calidad del ensamblaje y se realizan ajustes si es necesario.
Una read es una secuencia corta de
nucleótidos que se generan en una secuenciación
de ADN
NGS:Permiten la secuenciación en paralelo de un gran numero de fragmentos de ADN
1. Segmentación de ADN
2. Marcaje del ADN por medio de primers
3. Amplificación de fragmentos de ADN
mediante PCR
4. Secuenciación de los fragmentos
5. Reconstrucción de la secuencia completa por medio de secuencias de referencia
y exportación a ficheros de almacenamiento de datos