realizată de SantanaGamer 323 4 ani în urmă
363
Organigrama arbol
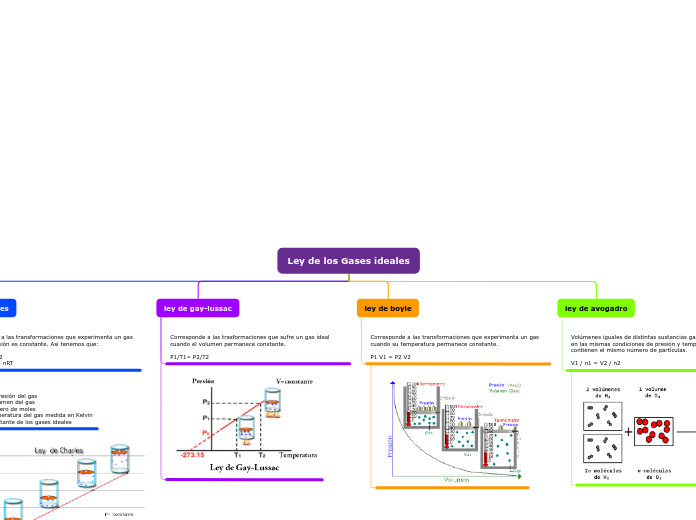
Las leyes de los gases ideales explican el comportamiento de los gases bajo diferentes condiciones. La ley de Boyle describe cómo un gas se transforma a temperatura constante, indicando que la presión y el volumen son inversamente proporcionales.