по BRENDA BERENICE VARGAS CASILLAS 4 лет назад
714
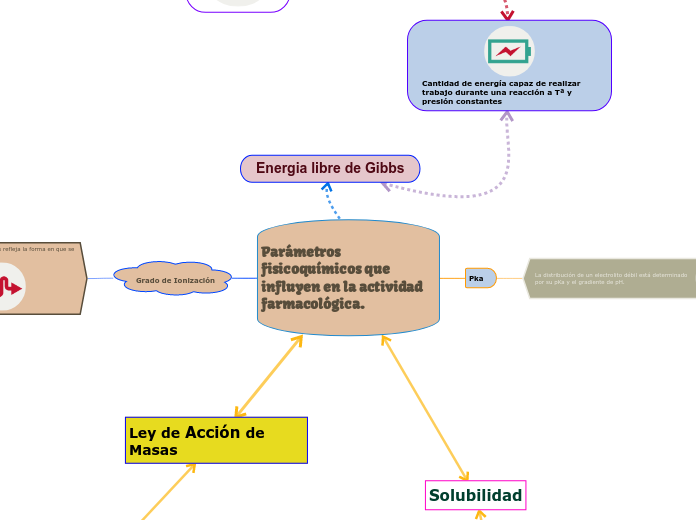
Parámetros fisicoquímicos que influyen en la actividad farmacológica.
En el estudio de la farmacología, uno de los conceptos fundamentales es la solubilidad, que se refiere a la capacidad de una sustancia para disolverse en otra. Este proceso está influenciado por la variación de la energía libre de Gibbs (