TIPOS DE REACCIONES QUÍMICA
Proceso químico de oxidación rápida
Tipos de combustión
combustión incompleta
Compuestos medio oxidados
Partículas de carbono
Hidrogeno
Monóxido de carbono (CO)
Combustión estequiométrica
Ocurre en el momento
El metano se transforma en CO2 Y H2O
Generalmente ocurre en un laboratorio controlado
Combustión completa
Esto pasa cuando
El material combustible se oxida por completo y se consume
Se desarrolla
Fase heterogénea
Fase gaseosa
Reversibles
Proceso que se dan en dos sentidos
Mezcla de reactivos y productos
También llamada equilibrio químico
N2O4 -> 2 NO 2
Ecuación general
A + B 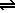 C + D
C + D
Solo hay dos reactivos, A y B
Irreversibles
Reacción química en un solo sentido
Cambios químicos reseñable
Disolución de metales
Neutralización acido de base fuertes
Combustiones
CO2, H2O, NO2 Y SO2
Oxidaciones
Representada por una simple ecuación
A + B -> C + D
A + B 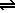 C + D
C + D
De óxido-reducción
2C8H18 + 25O2 -> 16CO2 + 18H2O
Transferencia de electrones
Pérdida de electrones
Aumenta su numero de oxidación
Proceso llamado Oxidación
Ganancia de electrones
Disminuye su numero de oxidación
La mezcla de potasio y agua
Todas las formas de
Oxidación
Combustión
Libera energía en forma de calor o luz al ambiente
Los productos obtenidos tienen menor energía
La mayoría de estas reacciones son de oxidación
También llamada
Reacción de desplazamiento
Implica el desplazamiento de un compuesto
ZN(S) + 2HCl(aq) -> 2 h2(g) + ZnCl2(aq)
Predicción y determinación de los productos
Topic principal
Exotérmicas
Cuando este tipo de reacción ocurre, los productos
obtenidos tienen menor:
Energía que los reactivos iniciales.
Ejemplos:
La combustión.
La mezcla de potasio y agua.
Una reacción exotérmica es aquella que cuando
ocurre libera:
Energía en forma de calor o luz al ambiente.
Sustitución simple
Una tira de cobre sumergida en una solución de nitrato de
plata desplazará
Átomos de plata
Produciendo
Precipitación de cristales del metal plata.c
Una reacción de sustitución simple, también llamada:
Reacción de desplazamiento simple
En la que un elemento se sustituye por otro dentro un
compuesto.
Cuando ocurre una reacción de sustitución, se generan
como productos:
Neutralización
Ecuación general de esta reacción
acido + base -> sal + agua
Reacción entre disoluciones ácidas y básicas
Endotérmicas
Ejemplo
Producción de ozono en la atmósfera
30 2(g) + energía (luz ultravioleta)
Reacción química que necesita energía calórica
Tienen un uso común en la industria
DE
Enfriamiento
Hielo químico
Dan como producto una sal y agua
Ácido sulfúrico y el hidróxido de sodio
H2SO4 + 2 NaOH -> Na2SO4 + 2 H2O
Síntesis
Descomposición
Producida por
Hidrólisis
CuSO4°5H2O -> CuSO4 + 5H2O
Electrólisis
2 NaCl -> 2 Na + Cl
Descomposición Térmica
CaCO3 -> CaO + CO2
Compuesto que forma dos o mas sustancias
Formula: AB -> A + B
Donde A y B representan dos sustancias
Se puede encontrar en
Sustancias inorgánicas
Importante a nivel industrial
Permite obtener sustancias que en forma natural ni existen
Na2O + H20 -> 2Na(OH)
2H2 + O2 -> 2H20
Ejemplos
El broce
Síntesis de cobre, estaño y a veces níquel
El acero
Sintesis de hierro y carbono
Sustancias orgánicas
Laboratorios
Ejemplos: Base de las industrias
Alimenticias
Cosméticos
Farmacéuticas
Naturaleza
Ejemplos: Organismos vivos
Proceso básico de la química
Para obtener un compuesto químico
Sustitución doble
Metástasis
Sin cambios en los números de oxidación
Por lo tanto
No son Reacciones Redox
Doble desplazamiento
2 elementos en compuestos diferentes
Forman nuevos compuestos
Ejemplo: AB+CD-->CB+AD
Los elementos A y C intercambian posiciones
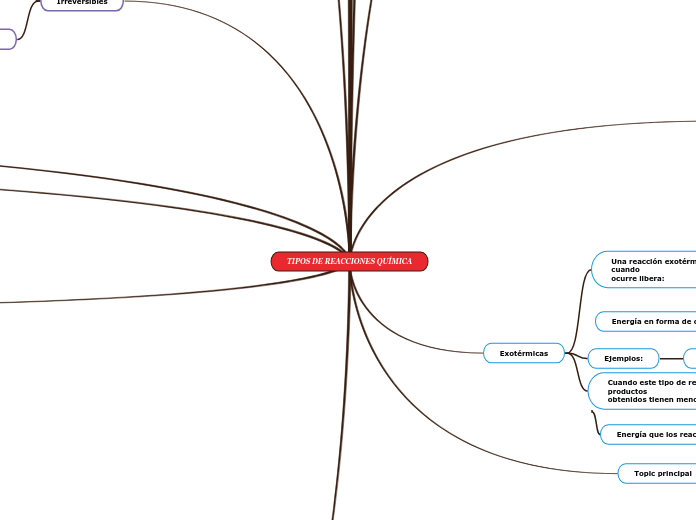


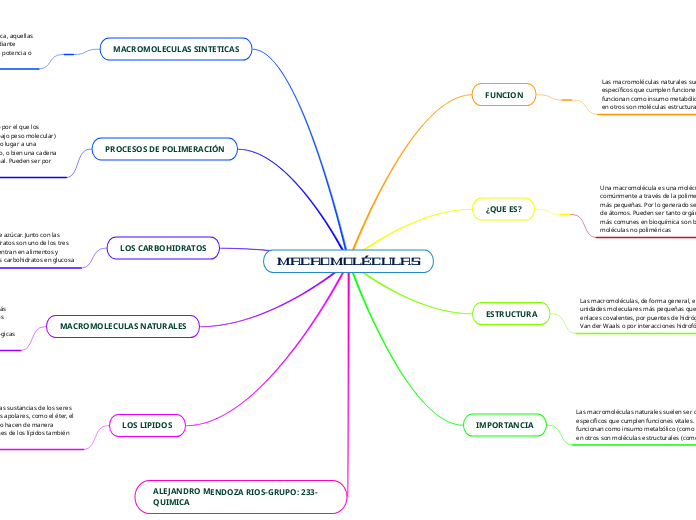

 C + D
C + D


