af samara romero herrera 5 år siden
278
Organigrama
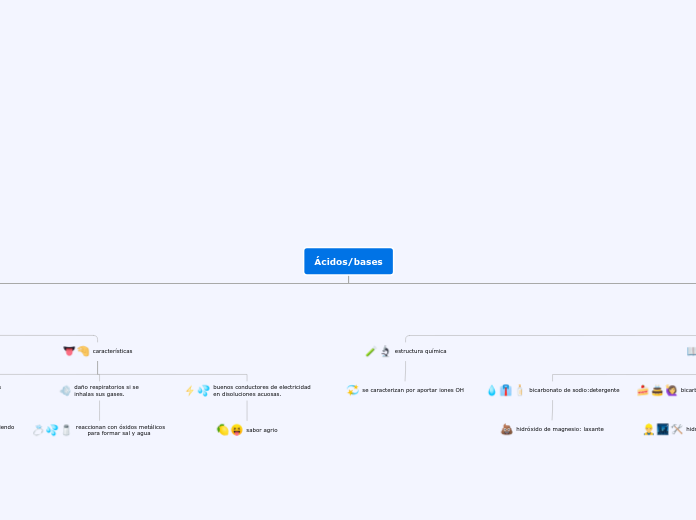
Las bases y los ácidos presentan propiedades químicas y físicas distintivas que determinan sus aplicaciones en diversos campos. Las bases, por ejemplo, tienen un sabor amargo característico, son buenos conductores de electricidad en soluciones acuosas y son solubles en agua.