Topic flotante
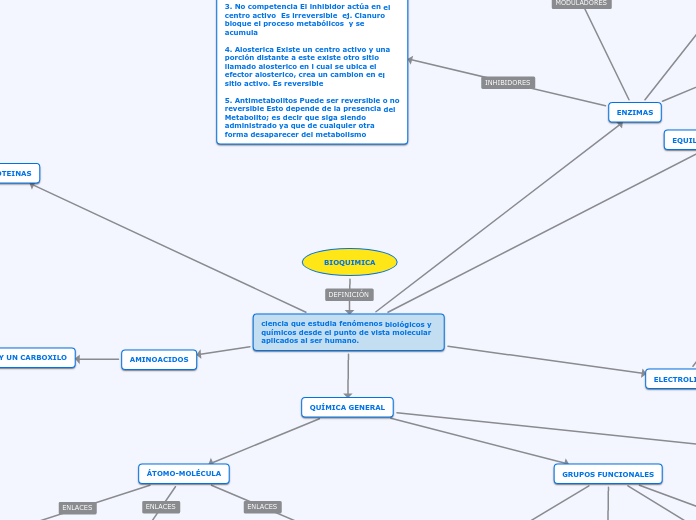
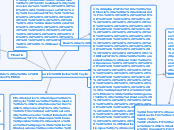
BIOQUIMICA
ciencia que estudia fenómenos biológicos y químicos desde el punto de vista molecular aplicados al ser humano.
ENZIMAS
1. iónica
2. por competencia Aparece estructura muy parecida al sustrato la cual ocupa el lugar de este en el sitio activo Es reversible si aumenta la cantidad e sustrato Sirve como mecanismo de regulación
3. No competencia El inhibidor actúa en el centro activo Es irreversible ej. Cianuro bloque el proceso metabólicos y se acumula
4. Alosterica Existe un centro activo y una porción distante a este existe otro sitio llamado alosterico en l cual se ubica el efector alosterico, crea un cambion en el sitio activo. Es reversible
5. Antimetabolitos Puede ser reversible o no reversible Esto depende de la presencia del Metabolito; es decir que siga siendo administrado ya que de cualquier otra forma desaparecer del metabolismo
Modulado negativo: inhibe la reacción, limita o inhibe la unió enzima-sustrato. Modulador positivo o activo: ayuda a la reacción, facilita o permite la unión enzima-sustrato
Oxidoreductasas: catalizan la transferencia de electrones o átomos de hidrogeno entre diferentes sustratos. 2. Ligasas: Catalizan unión. Utilizan la energía ATP. 3. Liasas: Catalizan la rotura de enlaces. Rompen sustratos catabólicos. Utilizan la energía ATP. 4. Hidrolasas: Catalizan la rotura de enlaces por medio de la introducción de moléculas de agua. Utilizan la energía ATP. 5. Transferasas: Catalizan la transferencia de grupos diferentes de hidrogeno C,O,N,P y S 6. Isomerasas: Catalizan el cambio de estructura, hay in re-arreglo intramolecular
Catalizador orgánico
PROTEINAS
SON POLIPEPTIDOS
CUATERNARIAS
Ningún enlace Ocurre polimerización: dímero, trímero, tetrámero…
TERCIARIAS
Enlace: de cualquier tipo (solo uno) Puente de hidrogeno. Entre aminos de –aminoácidos Atracción polar Fuerzas de Vander waals: aparece una complementariedad entre las estructuras y se acomodan Puentes di sulfuro Atracción electrostática tipo salino Tiene estructura primaria y secundaria. Son tridimensionales=es un monómero Tiene forma esférica o globular
SECUNDARIAS
Enlace: puente de hidrogeno -hélice o espiral laminar Simétrico Asimétrico Colágeno: triple hélice (2 hélices al mismo lado y 1 a la izquierda)
PRIMARIAS
Enlace: peptídico o covalente Tienen estructura lineal Péptidos unidos mediante unión peptídica =dipéptido
AMINOACIDOS
UN GRUPO AMINO Y UN CARBOXILO
NO ESENCIALES
SOLO EL CUERPO MISMO
arginina, cisteína, glutamina, tirosina, glicina, ornitina, prolina y serina.
ESENCIALES
PROVIENEN DE ALIMENTOS
histidina, isoleucina, leucina, lisina, metionina, fenilalanina, treonina, triptófano y valina.
EQUILIBRIO ÁCIDO-BASE
TAPONES
CONTRIBUYEN A LA REGULACION: ALBUMINA
USAMOS LA ECUACION DE HENDERSON HASELBACH PARA ECONTRAR EL PKa MAS PARECIDO AL PH SANGUINEO
SIST. RESPIRATORIO
AUMENTA O DISMINUYE LA FRECUENCIA RESPIRATORIA PARA REGULAR LA PCO2
ACIDOSIS Y ALCALOSIS METABOLICAS
SIST. RENAL
DISMINUYE LA SECRECION Y AUMENTA LA REABSORCION DE HCO3-
ACIDOSIS Y ALCALOSIS RESPIRATORIAS
ELECTROLITOS
PRIMARIOS
99% del peso corporal total CHON y Ca y P con una función estructural.
SECUNDARIOS
.7-.9% Na, Cl K Ca S y Mg
OLIGOELEMENTOS
.3-.1% Aparecen en cantidades mínimas, unidos a otros elementos para formar compuestos. Cu, Zn, Mo I, Fe
QUÍMICA GENERAL
AGUA
COLOGATIVAS
COLIGATIVAS
PUNTO EBULLICIÓN Y FUSIÓN,PUNTO CRIOSCOPICO, PRESION OSMOTICA Y DE VAPOR
PRESION OSMOTICA
PRESION DADA POR LA FUERZA QUE EJERCEN LOS SOLUTOS SOBRE EL AGUA
ELECTROLITOS, PROTEINAS, GLUCOSA
285-310 MOSMOLES
EQUILIBRIO DOWNAN EXPLICA LA EQUIVALENCIA DE OSMOLARIDAD DENTRO Y FUERA CELULA
FISIOLOGICAS
CAPILARIDAD, ADHESION, NO VISCOSA, TENSIO SUPERFICIAL, DENSIDAD
FISICOQUIMICAS
METABOLISMO H2O
INGESTA: 300ml /24hr (metabolismo) 1200 ml de agua visible 1000 ml de agua no visible
PERDIDAS:Vía insensible 400-600ml
Sudor 50-100ml
Heces 50-100ml
Orina +300ml al día
ANFOTERA, QUIMICAMENTE INHERTE, SOLVENTE UNIVERSAL, TERMICAS: CALOR ESPECIFICO, CONDUCTIVIDAD TERMICA.
ANFOTERISMO: AGUA SE DISOCIA EN H+ O OH-
PH PLASMA: 7.35-7.45
GRUPOS FUNCIONALES
AQUINOS
ENLACES TRIPLES
ALCOHOL
RADICAL HIDROXILO -OH
ALQUENOS
ENLACES DOBLES
ALCANOS
ENLACES SIMPLES
ÁTOMO-MOLÉCULA
PUENTES DE HIDROGENO
TENSIÓN SUPF. Y CAPACIDADES BIPOLARES POR EL AGUA
COVALENTE
COMPARTEN EL ELECTRON
CÉLULA
MITOCONDRIAS
MEMBRANA
BICAPA DOBLE LIPIDICA: DIGLICERIDOS Y FOSFOLIPIDOS
tienen un extremo hidrofobico y uno hidrofilico (antipáticos) crean la barrera de la membrana
MICELA:solubilizar lípidos, superficie de contacto incrementada (jabón) permite la adsorción y la absorción
MOSAICO FLUIDO: PROTEINAS INTEGRALES Y DIGLICERIDOS Y FOSFOLIPIDOS
APARATO GOLGI
LISOSOMAS
IONICO
UNO GANA ELECTRON