ESTRUCTURA Y PROPIEDADES DE LOS COMPUESTOS ORGÁNICOS
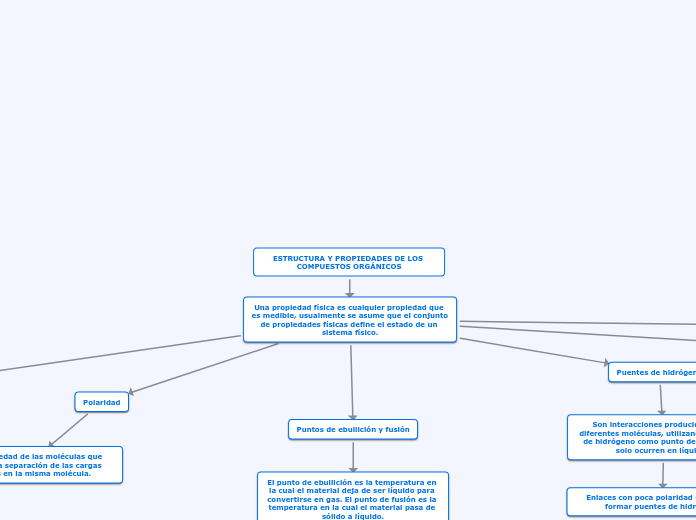
Una propiedad física es cualquier propiedad que es medible, usualmente se asume que el conjunto de propiedades físicas define el estado de un sistema físico.
Factores que afectan a las propiedades físicas
Ramificaciones
A medida que aumenta el # de cadenas secundarias en una estructura, se asume cierta forma esférica, y la molécula demuestra más independencia con respecto a sus vecinas, disminuye las interacciones entre las partículas.
La presencia de ramificaciones disminuye el punto d ebullición y aumenta solubilidad.
Masa molecular
El aumento en MM a medida que aumenta el # de C en la cadena principal, se produce una aumento de la temperatura de fusión y de ebullición, y en la densidad.
Efecto indutivo
Es la influencia de los sustituyentes, debido a la polarización
permanente de un enlace.
En la medida que un compuesto se polar, aumentan las interacciones entre sus moléculas, y por lo tanto, sus
propiedades físicas; tendrá mayor punto de fusión, de ebullición y solubilidad en agua o solvente polar.
En la mayoría de los compuestos orgánicos el átomo de carbono se enlaza a átomos más electronegativos, lo
que promueve que los electrones del enlace covalente sean atraídos con mayor intensidad hacia el átomo más
electronegativo.
Solubilidad
Cantidad de soluto que se disuelve en 100g de solvente a una temperatura determinada
las sustancias polares se
disuelven en disolventes polares y las no polares en disolventes no polares.
Puentes de hidrógeno
Son interacciones producidas entre diferentes moléculas, utilizando un átomo de hidrógeno como punto de enlace que solo ocurren en líquidos
Enlaces con poca polaridad no pueden formar puentes de hidrógeno
Polaridad
Es una propiedad de las moléculas que representa la separación de las cargas eléctricas en la misma molécula.
Puntos de ebullición y fusión
El punto de ebullición es la temperatura en la cual el material deja de ser líquido para convertirse en gas. El punto de fusión es la temperatura en la cual el material pasa de sólido a líquido.
Mientras que la intensidad de las interacciones aumenten , los puntos de ebullicion y fusion seran mayores
Los isómeros ramificados tienen un punto de ebullición menor a los de los lineales
Los isómeros que presentan el grupo oxidrilo en los extremos presentan un punto de ebullición mayor a los que no son termianles
Densidad
Relación que existe entre la masa de un material y el volumen que ocupa
Mayor masa molecular = Mayor densidad
Mayo interacción molecular = Mayor densidad