I LEGAMI METALLICI
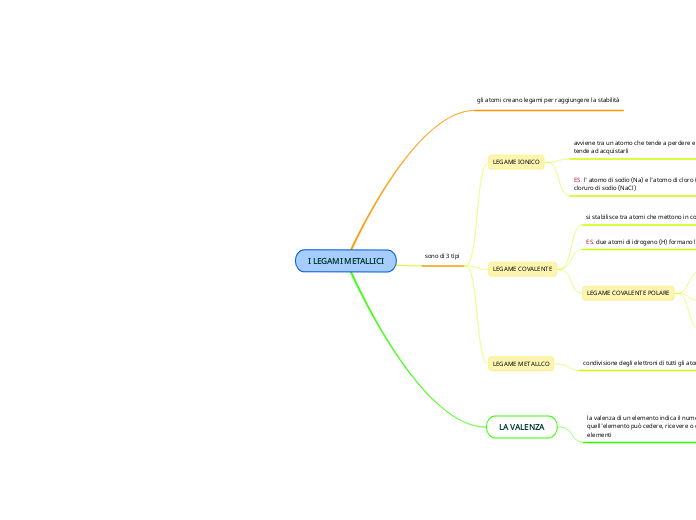
LA VALENZA
la valenza di un elemento indica il numero di elettroni che quell'elemento può cedere, ricevere o condividere con gli altri elementi
sono di 3 tipi
LEGAME METALLCO
condivisione degli elettroni di tutti gli atomi di un metallo
gli elettroni
vengono condivisi tra tutti gli atomi formando una "nuvola" elettronica delocalizzata
si trasformano in cationi
LEGAME COVALENTE
LEGAME COVALENTE POLARE
ES. 2 atomi di idrogeno (H) si legano a 1 atomo di ossigeno (O) formando l'acqua (H2O)
gli elettroni non si collocano in una posizione intermedia tra i nuclei, ma più vicino all'atomo che li attira con più forza
la molecola che ne risulta acquista una polarità elettronica
si instaura tra atomi diversi
ES. due atomi di idrogeno (H) formano la molecola di idrogeno
si stabilisce tra atomi che mettono in comune alcuni elettroni
gli atomi perciò
condividono gli elettroni finché entrambi hanno 8 elettroni nel guscio di valenza
LEGAME IONICO
ES. l' atomo di sodio (Na) e l'atomo di cloro (Cl) formano il cloruro di sodio (NaCl)
avviene tra un atomo che tende a perdere elettroni e uno che tende ad acquistarli
si formano 2 ioni
ione positivo
ione negativo
gli atomi creano legami per raggiungere la stabilità