Definición
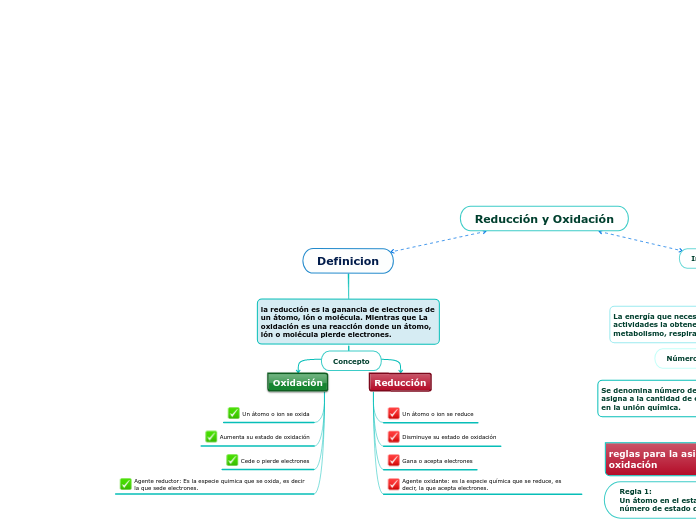
Reducción y Oxidación
EJERCICIO
En las siguientes reacciones realiza las semirreacciones y señala ¿Quién
se oxida y quien se reduce?, ¿Quién es el agente reductor y el agente
oxidante? Y ¿Cuántos electrones se transfieren en cada una de las
semirreacciones?
NH3 + H2SO4 S+ HNO3 + H2O
SO3 + MnO4- SO4+ Mn+2
Cr2O4=+Fe(OH)2 CrO2 + Fe (OH)3
Regla 4:
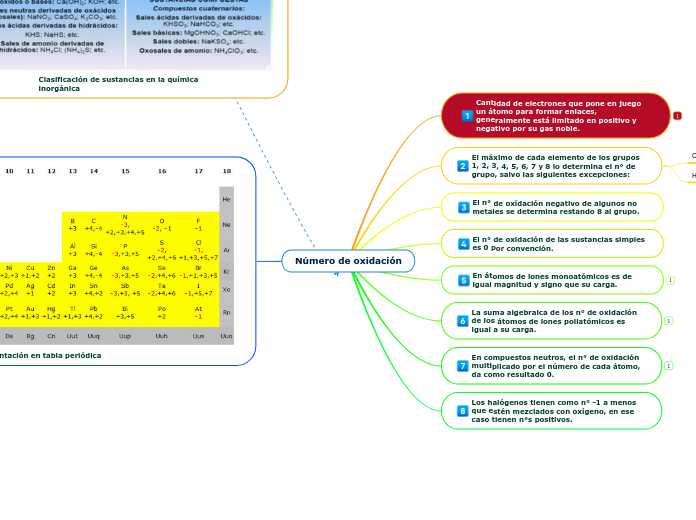
El número de oxidación de toda molécula simple o compuesta es cero.
Regla 3:
Los elementos del grupo IA tienen estado de oxidación +1
Los elementos del grupo IIA tienen estado de oxidación +2
Regla 2:
Como regla general para el hidrógeno y el oxígeno.
Regla 1:
Un átomo en el estado elemental tiene número de estado de oxidación cero.
Se denomina número de oxidación a la carga que se le asigna a la cantidad de electrones que cede o recibe en la unión química.
reglas para la asignación de número de oxidación
Número de Oxidación
La energía que necesitamos para realizar nuestras
actividades la obtenemos mediante Procesos de metabolismo, respiración celular.
Importancia
Concepto
Definicion
The advantages and disadvantages are the pros and cons of a certain topic, that each person considers thoroughly before making a bigger decision.
la reducción es la ganancia de electrones de un átomo, ión o molécula. Mientras que La oxidación es una reacción donde un átomo, ión o molécula pierde electrones.
Add here the topic you want to reflect on!
It can be a serious life-changing matter or even a decision on whether to buy a new car or not!
You can describe here why you need this decision or add any other considerations in this regard.
Reducción
Agente oxidante: es la especie química que se reduce, es decir, la que acepta electrones.
Gana o acepta electrones
Disminuye su estado de oxidación
Add your counterarguments here!
Un átomo o ion se reduce
Add your counterarguments here!
Oxidación
Agente reductor: Es la especie quimica que se oxida, es decir la que sede electrones.
Cede o pierde electrones
Aumenta su estado de oxidación
Un átomo o ion se oxida
Add your pro arguments here!