por santiago marque galeano 4 anos atrás
944
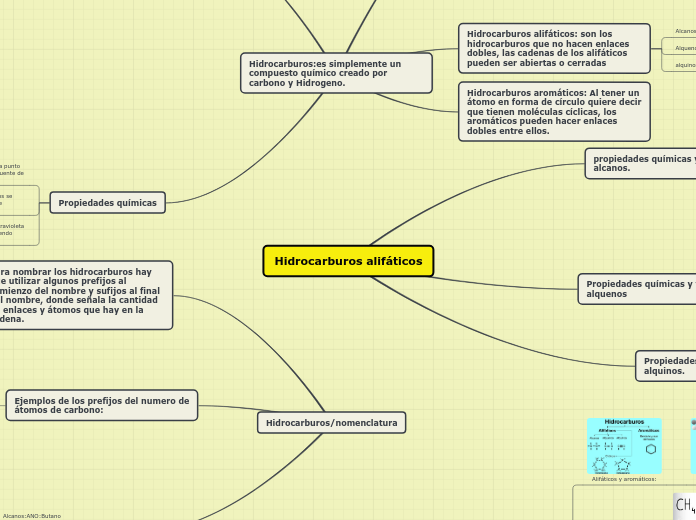
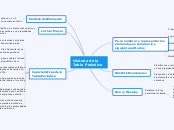
Hidrocarburos alifáticos
Los hidrocarburos alifáticos presentan diversas propiedades físicas y químicas dependiendo de su estructura. Los alquinos, considerados ácidos en presencia de bases fuertes, pueden ceder protones, y suelen ser líquidos, menos insolubles que alquenos y alcanos.