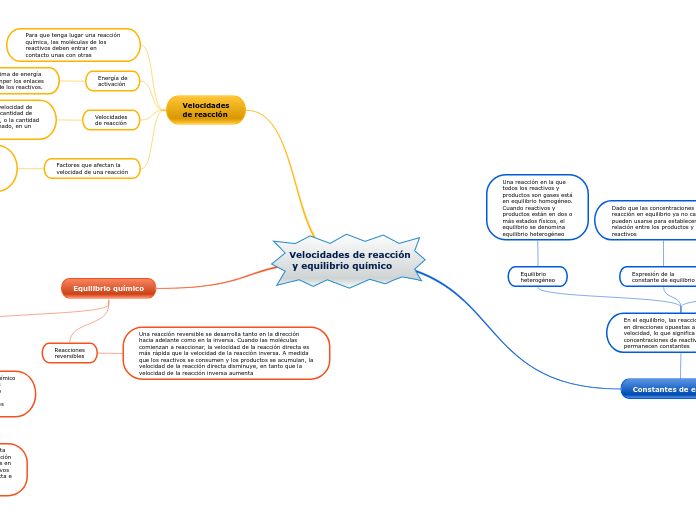
Velocidades de reacción
y equilibrio químico
Equilibrio químico
Reacciones
reversibles
Una reacción reversible se desarrolla tanto en la dirección hacia adelante como en la inversa. Cuando las moléculas comienzan a reaccionar, la velocidad de la reacción directa es más rápida que la velocidad de la reacción inversa. A medida que los reactivos se consumen y los productos se acumulan, la velocidad de la reacción directa disminuye, en tanto que la velocidad de la reacción inversa aumenta
Equilibrio
químico
Una reacción alcanza equilibrio químico
cuando no hay más cambio en las
concentraciones de los reactivos o
productos, incluso cuando las dos
reacciones continúen a velocidades
iguales pero opuestas.
La velocidad de la reacción directa
es igual a la velocidad de la reacción
inversa. No ocurren más cambios en
las concentraciones de los reactivos
o productos; las reacciones directa e
inversa continúan a velocidades
iguales.
Velocidades
de reacción
Factores que afectan la
velocidad de una reacción
La velocidad de cualquier
reacción se modifica si hay
cambios en la temperatura,
cambios en las concentraciones
de los reactivos y la adición de
catalizadores.
Para determinar la velocidad de
reacción se mide la cantidad de
un reactivo agotado, o la cantidad
de un producto formado, en un
lapso determinado
Energía de
activación
es la cantidad mínima de energía
necesaria para romper los enlaces
entre los átomos de los reactivos.
Para que tenga lugar una reacción
química, las moléculas de los
reactivos deben entrar en contacto unas con otras
Constantes de equilibrio
En el equilibrio, las reacciones ocurren
en direcciones opuestas a la misma
velocidad, lo que significa que las
concentraciones de reactivos y productos
permanecen constantes
Cómo calcular constantes
de equilibrio
El valor numérico de la constante
de equilibrio se calcula a partir de
la expresión de la constante de
equilibrio, al sustituir en la expresión
las concentraciones de los reactivos y
los productos en equilibrio medidas
experimentalmente
Expresión de la
constante de equilibrio
Dado que las concentraciones en una
reacción en equilibrio ya no cambian,
pueden usarse para establecer una
relación entre los productos y los
reactivos
Equilibrio
heterogéneo
Una reacción en la que
todos los reactivos y
productos son gases está
en equilibrio homogéneo.
Cuando reactivos y
productos están en dos o
más estados físicos, el
equilibrio se denomina
equilibrio heterogéneo