av Elia Infante för 5 årar sedan
575
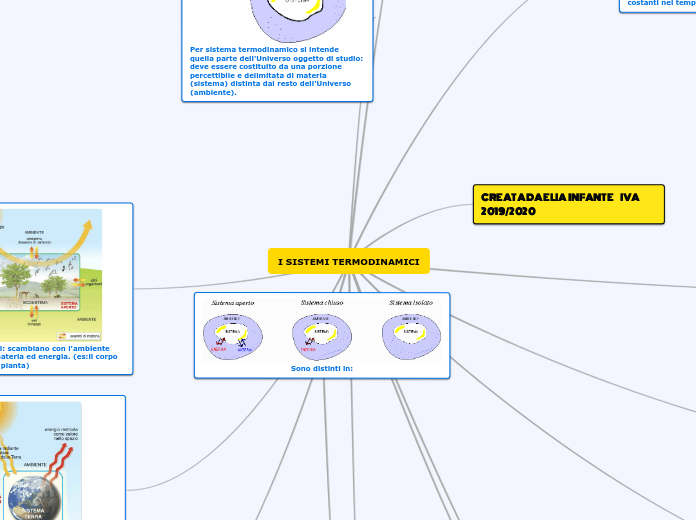
I SISTEMI TERMODINAMICI
I sistemi termodinamici sono studiati per comprendere le variazioni di energia interna e le interazioni con l'ambiente. I sistemi adiabatici, isolati e chiusi sono modelli teorici che descrivono differenti gradi di scambio di calore e materia con l'