作者:Juana Jaramillo 4 年以前
1362
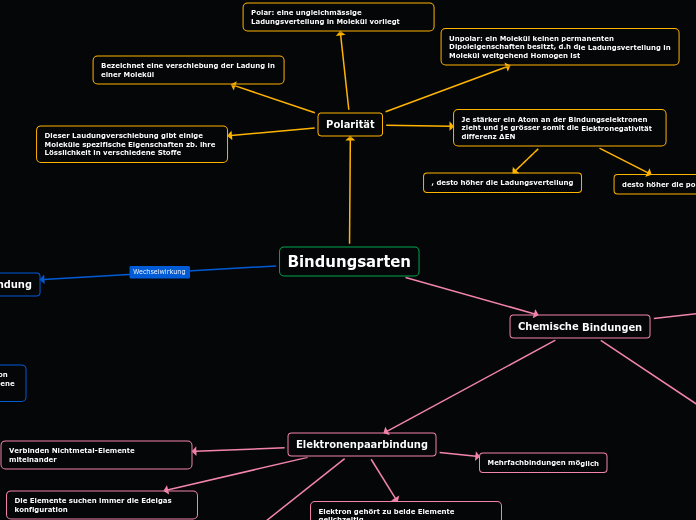
Bindungsarten
Die verschiedenen chemischen Bindungsarten spielen eine wichtige Rolle in der Chemie. Van-der-Waals-Kräfte sind schwache intermolekulare Kräfte, die auch bei unpolaren Molekülen wirken und die physikalischen Eigenschaften beeinflussen.
開啟
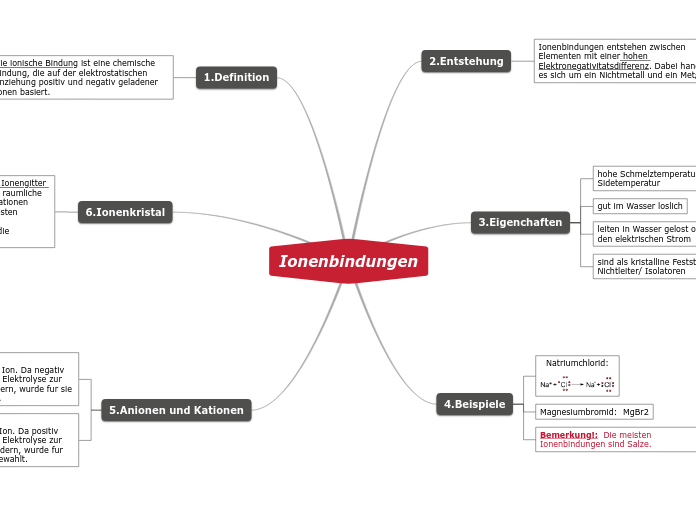
Bindungsarten Polarität Je stärker ein Atom an der Bindungselektronen zieht und je grösser somit die Elektronegativität differenz ΔEN desto höher die polarität , desto höher die Ladungsverteilung Unpolar: ein Molekül keinen permanenten Dipoleigenschaften besitzt, d.h die Ladungsverteilung in Molekül weitgehend Homogen ist Polar: eine ungleichmässige Ladungsverteilung in Molekül vorliegt Dieser Laudungverschiebung gibt einige Moleküle spezifische Eigenschaften zb. ihre Lösslichkeit in verschiedene Stoffe Bezeichnet eine verschiebung der Ladung in einer Molekül Chemische Bindungen Van-der-Waals-Kräfte Drei Arten: Dipol-Dipol (stark), induziertes Dipol-Dipol (ittlere stärke), unpolare Moleküle(Dispersionskräfte) (niedrige starke) Ladungsverteilung unsymetrisch Beeinflussen physikalischem Eigenschaften Wirkt auch bei unpolaren Moleküle Kraft zwischen ein Dipol und ein induzierte Dipol Es ist eine intermolekülare Kräfte Ionenbindung Eine Ionen gitter wird durch die anziehung zwischen alle Ion Elektrostatisch anziehungs Kraft Die Elektrondifferenz muss grosser als 1,7 sein, damit es eine Ionbindung besteht Elektronenkette wird erreicht durch die Bindung von Kationen (positiv geladen) und Anionen (negativ geladen) Die Metallen geben ihre aussen Elektron ab Bindung von metalle und nichtmetalle (stark Bindung) Elektronenpaarbindung Mehrfachbindungen möglich Elektron gehört zu beide Elemente gelichzeitig Teilen sie sich die beiden Elementen die Valenzelektronen Die Elemente suchen immer die Edelgas konfiguration Verbinden Nichtmetal-Elemente miteinander Wasserstoffbrückenbindung Keine richitge Bindung, sonedrn atraktion zwischen positiven und negativen geladene Moleküle Passiert wenn die Elektronnegativität differenz zu gross ist Die Bindungs ist zwischen Moleküle mit wasserstoffatome Ist eine strake Bindung zwischen des Dipols der Molekül Sind keine wirkliche chemische Bindungen -> Wechselwirkung